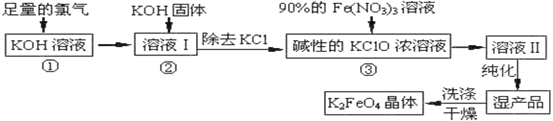
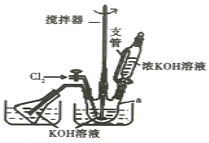
题目内容
【题目】按要求填空
(1)1mol Na2O2固体与水完全反应时转移的电子数_____________,反应的离子方程式为________________。
(2)工业上由辉铜矿生产铜的主要反应为:Cu2S+O2![]() 2Cu+SO2,该反应中被还原的元素是__________(填元素符号)。
2Cu+SO2,该反应中被还原的元素是__________(填元素符号)。
(3)反应(2)中产生的SO2尾气可用NaOH溶液吸收,若用1L 1mol/L的NaOH溶液吸收标准状况下22.4L SO2,反应的离子方程式为____________。
【答案】NA(或6.02×1023) 2Na2O2+2H2O=4Na++4OH-+O2↑ Cu、O SO2+OH-=HSO3-
【解析】
(1) Na2O2与水完全反应产生NaOH和O2,根据元素化合价与电子转移关系判断电子转移数目,结合离子方程式书写原则书写离子方程式;
(2)根据元素化合价的升降与发生的反应类型分析判断;
(3)根据SO2、NaOH的物质的量关系书写离子方程式。
(1) Na2O2与水完全反应产生NaOH和O2,反应方程式为:2Na2O2+2H2O=4NaOH+O2↑,在这个反应中,Na2O2中的O一部分化合价升高变为O2中的0价,一部分化合价降低,变为NaOH中的-2价,每有1molNa2O2反应,转移1mol电子,转移的电子数目为NA;该反应用离子方程式表示为:2Na2O2+2H2O=4Na++4OH-+O2↑;
(2)在该反应中Cu、O元素的化合价降低,获得电子被还原;
(3)n(NaOH)= 1L×1mol/L=1mol,n(SO2)=22.4L÷22.4L/mol=1mol,n(NaOH):n(SO2)=1:1,所以NaOH溶液吸收SO2的反应方程式为:SO2+OH-=HSO3-。

【题目】某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白。
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_______,直到因加入一滴盐酸后,溶液由________色变为________色,并________为止。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是__________。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
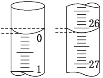
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则起始读数为_______mL,终点读数为_______mL,所用盐酸溶液的体积为_______mL。
(4)某学生根据3次实验分别记录有关数据如下表:
滴定 次数 | 待测NaOH溶液的体积/mL | 0.100 0 mol·L-1 盐酸的体积/mL | ||
滴定前读数 | 滴定后读数 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
依据上表数据列式计算该NaOH溶液的物质的量浓度__________________________。