题目内容
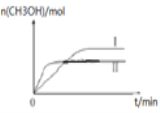
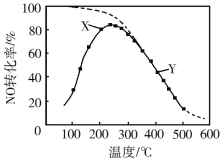
【题目】在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法不正确的是( )
A.反应2NO(g)+O2(g)=2NO2(g)的ΔH<0
B.图中X点所示条件下,延长反应时间能提高NO转化率
C.图中Y点所示条件下,增加O2的浓度不能提高NO转化率
D.380℃下,c起始(O2)=5.0×104mol·L1,NO平衡转化率为50%,则平衡常数K>2000
【答案】C
【解析】
A.根据图知,升高温度NO转化率降低,说明升高温度平衡逆向移动,升高温度平衡向吸热方向移动,则正反应为放热反应,△H<0,故A正确;
B.图中X点在该温度下没有达到平衡状态,此点反应正向移动,所以延长时间能提高NO转化率,故B正确;
C.Y点为该温度下的平衡点,增大反应物O2浓度,平衡正向移动,从而提高NO转化率,故C错误;
D.设消耗的c(O2)=xmol/L,根据方程式知,消耗的c(NO)=2c(O2)=2xmol/L,NO的转化率为50%,则c起始(NO)=4xmol/L,平衡时c(NO)=2xmol/L、c(NO2)=2xmol/L,c(O2)=(5.0×104-x)mol/L,化学平衡常数K=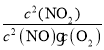 =
=![]() >2000,故D正确;
>2000,故D正确;
故答案选C。

练习册系列答案
相关题目