题目内容
【题目】某无色溶液X,由Na+、Mg2+、Ba2+、Al3+、AlO2-、MnO![]() 、CO
、CO![]() 、SO
、SO![]() 中的若干种离子组成,取溶液进行如下连续实验:
中的若干种离子组成,取溶液进行如下连续实验:
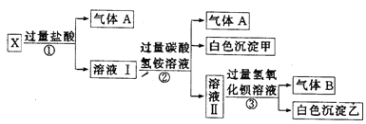
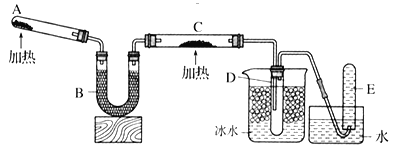
(1)气体A的成分是_______(填电子式),气体B的成分是_______(填结构式)
(2)X溶液中一定不存在的离子是______________。
(3)写出步骤①中发生反应的所有离子方程式:________________。
(4)写出步骤②中形成白色沉淀的离子方程式:________________。
(5)通过上述实验,溶液X中不能确定是否存在的离子是______________;只要设计一个简单的后续实验就可以确定该离子是否存在,该方法是__________________。
【答案】![]()
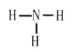 Mg2+、Ba2+、Al3+、MnO4- CO32-+2H+=H2O+CO2↑ AlO2-+4H+=Al3++2H2O,Al3++3HCO3-=Al(OH)3↓+3CO2↑ SO42- 在沉淀乙中加入足量盐酸,若白色沉淀能完全溶解,则X中不存在SO42-;若不完全溶解,则X中存在SO42-
Mg2+、Ba2+、Al3+、MnO4- CO32-+2H+=H2O+CO2↑ AlO2-+4H+=Al3++2H2O,Al3++3HCO3-=Al(OH)3↓+3CO2↑ SO42- 在沉淀乙中加入足量盐酸,若白色沉淀能完全溶解,则X中不存在SO42-;若不完全溶解,则X中存在SO42-
【解析】
溶液呈无色,则一定不含MnO4-,溶液X中加入过量盐酸,有气体A生成,并得到溶液I,说明原溶液中含有CO32-,气体A为CO2,CO32-与Mg2+、Ba2+、Al3+不能大量共存,则原溶液一定不含Mg2+、Ba2+、Al3+;反应①中加入盐酸过量,反应②中加入过量的NH4HCO3,产生的气体为CO2,白色沉淀甲只能为Al(OH)3,则X溶液中一定含有AlO2-,碳酸氢铵过量,与过量Ba(OH)2反应并加热,得到气体为NH3,白色沉淀乙一定含有BaCO3,可能含有BaSO4,所以溶液X中一定不存在的离子有:MnO4-、Mg2+、Ba2+、Al3+,不能确定原溶液中是否含有SO42-,根据溶液电中性原则可知含有Na+,溶液X中一定含有CO32-、AlO2-、Na+,以此分析解答。
(1)由分析可知,气体A为CO2,CO2为共价化合物,碳原子和每个氧原子之间有两个共用电子对,电子式为:![]() ;气体B为NH3,氮原子和每个氢原子之间有一个共用电子对,结构式为:
;气体B为NH3,氮原子和每个氢原子之间有一个共用电子对,结构式为: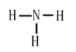 ;
;
(2)由分析可知,X溶液中一定不存在的离子是Mg2+、Ba2+、Al3+、MnO4-;
(3)步骤①X溶液中加入过量盐酸,碳酸根与盐酸反应生成二氧化碳气体,离子方程式为:CO32-+2H+=H2O+CO2↑;
(4)由分析可知X中有AlO2-,与盐酸反应生成Al3+,铝离子和碳酸氢根离子水解相互促进生成二氧化碳气体和氢氧化铝白色沉淀,有关的离子方程式:AlO2-+4H+=Al3++2H2O,Al3++3HCO3-=Al(OH)3↓+3CO2↑;
(5)由分析可知,不能确定溶液X中是否含有SO42-,要验证SO42-的存在,根据BaCO3不溶于水但能溶于酸、BaSO4既不溶于水也不溶于酸的性质,可在沉淀乙中加入足量盐酸,若白色沉淀能完全溶解,则X中不存在SO42-;若不完全溶解,则X中存在SO4-,答案为:SO42-;在沉淀乙中加入足量盐酸,若白色沉淀能完全溶解,则X中不存在SO42-;若不完全溶解,则X中存在SO4-。

 阅读快车系列答案
阅读快车系列答案【题目】经测定乙醇的分子式是![]() ,由于有机化合物普遍存在同分异构现象,推测乙醇分子的结构可能是下列两种之一:
,由于有机化合物普遍存在同分异构现象,推测乙醇分子的结构可能是下列两种之一:
Ⅰ.  Ⅱ.
Ⅱ. 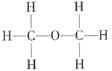
为确定其结构,应利用物质的特殊性质进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,甲、乙、丙三名学生利用如图所示装置进行实验确定乙醇分子的结构。图中量气装置由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水。甲管有刻度(0~200mL),供量气用;乙管可上下移动,以调节液面高低。

(1)学生甲得到一组实验数据;
乙醇的物质的量 | 氢气的体积(标准状况下) |
0.01mol | 0.112L |
根据以上数据推断,乙醇的结构应为___________________(填“Ⅰ”或“Ⅱ”),原因是_______________
(2)学生乙认为:为了较准确地测量氢气的体积,除了必须检查整个装置的气密性外,在读取反应前后甲管中液面读数的过程中,应注意___________________(填序号)。
a.视线与凹液面最低处相平
b.等待片刻,待乙管中液面不再上升时,立刻读数
c.读数时应上下移动乙管,使甲、乙两管液面相平
d.读数时不一定使甲、乙两管液面相平