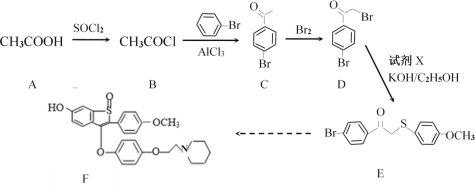
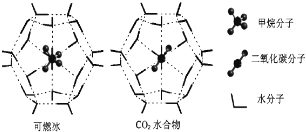
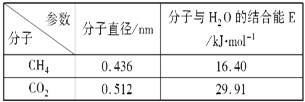
��Ŀ����
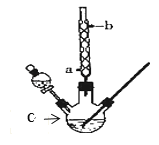
����Ŀ��ij��ѧ����С���������ͼ��ʾ��װ����ȡ����������ͼ�мг������ͼ���װ������ȥ������֪�������ݣ�
�Ҵ� | ���� | �������� | 98%Ũ���� | |
�۵�/�� | ��117.3 | 16.6 | ��83.6 | |
�е�/�� | 78.5 | 117.9 | 77.5 | 338.0 |
��ش��������⣺
(1)����C������Ϊ______�����������ܵ�������_____��
(2)��C�м��뷴Ӧ�����ַ�Ӧ��C�еĻ���ﵹ��װ�б���̼������Һ���ձ��г����ϴ�ӡ�����̼������Һ�����ǣ�����ĸ����_____
A.�к����Ტ�ܽ��Ҵ�
B.̼������Һ�ʼ��ԣ�����������������ˮ��
C.�����������������ɣ���������
D.���������ڱ���̼������Һ�е��ܽ�ȱ���ˮ�и�С�������ڷֲ�����
(3)�������ϴ�ӡ����÷�Һ��Ϊ�˽�һ���ᴿ�����������ɲ�������ķ���������ʱ�����¶���__���ң��¶ȼƵ�ˮ����Ӧλ��____��
(4)��ʵ��������������Ϊ2.4g���Ҵ�����Ϊ2.1g���õ������IJ�Ʒ����Ϊ2.64g�������������IJ�����______��
(5)��������������������Һ������Ӧ�Ļ�ѧ����ʽΪ____________��
���𰸡�������ƿ �������� AD 77.5�� ��֧�ܿ�ƽ�� 75% CH3COOC2H5+NaOH![]() CH3COONa+CH3CH2OH
CH3COONa+CH3CH2OH
��������
(1)����C������Ϊ������ƿ�����������ܵ��������������������ԭ�������ʣ�
(2)����������ԣ��ܺͱ���̼������Һ��Ӧ���ѱ����գ����������ڱ���̼������Һ�е��ܽ�Ƚ�С��
(3)���ݱ������ݿ�֪��������������ķе�Ϊ77.5�棬�¶ȼƵ�ˮ����Ӧλ��֧�ܿ���ƽλ�ã���ʱ������¶�Ϊ����¶ȣ�
(4)������Ҵ��ķ�ӦΪCH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O��2.4g�����2.1g�Ҵ����ʱ��֪�Ҵ�����������2.4g��������������������۲��������ò���=
CH3COOCH2CH3+H2O��2.4g�����2.1g�Ҵ����ʱ��֪�Ҵ�����������2.4g��������������������۲��������ò���=![]() ��100%���㣻
��100%���㣻
(5)��������������������Һ������ȫˮ�ⷴӦ�����ɴ����ƺ��Ҵ����ݴ�д����ѧ����ʽ��
(1)����C������Ϊ������ƿ�����������ܵ��������������������ԭ�������ʣ�
(2)����������ԣ��ܺͱ���̼������Һ��Ӧ���ѱ����գ����������ڱ���̼������Һ�е��ܽ�Ƚ�С�����ڷ��룬�ʺ���ѡ����AD��
(3)���ݱ������ݿ�֪��������������ķе�Ϊ77.5�棬�����ռ���ƷӦ�����¶���77.5�����ң������¶ȼƵ�ˮ����Ӧλ��֧�ܿ���ƽλ�ã�������¶Ȳ�������¶ȣ�
(4)������Ҵ��ķ�ӦΪCH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O����Ϊ60��46��2.4��2.1������2.4g�����2.1g�Ҵ����ʱ���Ҵ�������2.4g���������������������۲���=
CH3COOCH2CH3+H2O����Ϊ60��46��2.4��2.1������2.4g�����2.1g�Ҵ����ʱ���Ҵ�������2.4g���������������������۲���=![]() ��88g=3.52g�����������IJ���=
��88g=3.52g�����������IJ���=![]() ��100%=75%��
��100%=75%��
(5)��������������������Һ������ȫˮ�ⷴӦ�����ɴ����ƺ��Ҵ�����ѧ����ʽΪCH3COOC2H5+NaOH=CH3COONa+CH3CH2OH��

 �����Ƹ���ʦ����ϵ�д�
�����Ƹ���ʦ����ϵ�д� ��ͨ����ͬ����ϰ��ϵ�д�
��ͨ����ͬ����ϰ��ϵ�д�����Ŀ���±�ΪԪ�����ڱ���һ���֣������Ԫ�آ٣����ڱ��е�λ�ã�����ѧ�����ش��������⣺
�� ���� | IA | 0 | ||||||
1 | �� | ��A | ��A | ��A | ��A | ��A | ��A | |
2 | �� | �� | �� | �� | ||||
3 | �� | �� | �� | �� | ||||
(1)ԭ�Ӱ뾶��С��Ԫ����____����Ԫ�����ƣ���д�����ԭ�ӽṹʾ��ͼ______��
(2)����������Ӧ��ˮ�����У�������ǿ����___���û�ѧʽ�ش���ͬ����������ǿ����___��
(3)������γɵĻ������У���ѧ������Ϊ_____��
(4)������γɵĻ�����ĵ���ʽΪ___��������γɵ�ԭ�Ӹ�����Ϊ1:2�Ļ�����ĽṹʽΪ____��
(5)�ۡ��ܡ���ԭ�Ӱ뾶�ɴ�С��˳��Ϊ_____����Ԫ�ط��Żش𣩡�
(6)Ϊ̽��Ԫ�آں͢�ķǽ�����ǿ����ijͬѧ�������ͼ��ʾ��װ�ý���ʵ�飨�г���������ȥ��װ�����������ã�����ش�
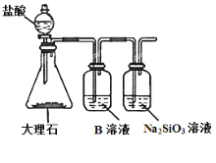
a.��ҺB��������_______
b.������____������֤������_______���û�ѧʽ�ش𣩣���ǽ�����_______����Ԫ�ط��Żش𣩡�
c.����ʵ���У���˵���ں͢�ǽ�����ǿ���Ļ�ѧ����ʽ��_____________��