题目内容
2.下列各反应中,符合如图所示能量变化的是( )
| A. | 金属钠与水的反应 | B. | 氢氧化钡晶体与氯化铵混合反应 | ||
| C. | 氧化钙与水的反应 | D. | 酒精燃烧 |
分析 图象分析可知反应物能量低于生成物,反应是吸热反应,分析选项选择即可.
解答 解:A、金属钠与水反应生成氢氧化钠和氢气,反应是放热反应,故A不符合;
B、氢氧化钡晶体「Ba(OH)2•8H2O」与氯化铵晶体混合反应过程是吸热反应,故B符合;
C、氧化钙与水反应生成氧化钙,发生的是化合反应,反应放热,故C不符合;
D、酒精在氧气中燃烧是放热反应,故D不符合;故选B.
点评 本题考查了化学反应能量变化分析判断,掌握反应特征和反应过程中能量变化是解题关键,题目较简单.

练习册系列答案
相关题目
10.常温下,下列溶液中的离子浓度关系一定正确的是( )
| A. | PH=11的Na2SO3溶液中,水的电离c( H+)=1.0×10-11mol/L | |
| B. | PH=10的某BOH的碱溶液中加水稀释至100倍,稀释后的溶液中c( OH-)=1.0×10-6mol/L | |
| C. | PH=4的NaHC2O4溶液中存在:c( Na+)>c(HC2O4-)>c( H+)>c(C2O42-)>c( OH-) | |
| D. | PH=2的硝酸与PH=12的氨水等体积混合c( NO3-)>c( NH4+)>c( H+)>c( OH-) |
17.下列化合物中,属于原子晶体的是( )
| A. | CO2 | B. | NaOH | C. | SiO2 | D. | Si |
7.相同温度和压强下,在容积为2L的密闭容器中发生反应:2HI(g)?H2(g)+I2(g),达到平衡状态的标志是( )
| A. | c(H2)保持不变 | |
| B. | 拆开2 mol H-I共价键,同时生成1 mol H-H共价键 | |
| C. | HI、H2、I2的浓度比为2:1:1 | |
| D. | 正反应和逆应都已停止 |
14.下列说法中,错误的是( )
| A. | 化学反应必然伴随着能量的变化 | |
| B. | 能量变化是化学反应的基本特征之一 | |
| C. | 化学变化的能量变化主要是由化学键的变化引起的 | |
| D. | 化学反应中能量变化的大小与反应物的状态和物质的量无关 |
11.下列除去杂质(括号内为杂质)的方法中,正确的是( )
| A. | NO(NO2):通过装有水的洗气装置 | |
| B. | Cu粉(铁粉):加足量稀硝酸,过滤 | |
| C. | NH3(H2O):通过装有浓硫酸的洗气装置 | |
| D. | KCl(CaCl2):加适量Na2CO3溶液,过滤 |
12.某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol•L-1 FeCl2溶液,实验记录如表(a、b、c代表电压值):
(1)用KSCN溶液检验出溶液中含Fe3+,看到的现象是溶液变红.
(2)Ⅰ中,Fe3+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化.写出Cl2氧化Fe2+的离子方程式:Cl2+2Fe2+═2Cl-+2Fe3+.
(3)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电.原因是Fe2+具有还原性.
(4)Ⅱ中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证.控制变量,做对照实验继续探究:电解pH=1的NaCl溶液,记录如表:
①NaCl溶液的浓度应是0.2 mol•L-1.
②Ⅳ中检验Cl2的实验方法:取少量阳极附近的溶液,滴在淀粉碘化钾试纸上,试纸变蓝色.
③与Ⅱ对比,得出的结论:通过控制电压,证实了产生Fe3+的两种原因都成立;通过控制电压,验证了放电顺序是:Fe2+>Cl-(填“>”或“<”)
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅰ | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| Ⅱ | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| Ⅲ | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
(2)Ⅰ中,Fe3+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化.写出Cl2氧化Fe2+的离子方程式:Cl2+2Fe2+═2Cl-+2Fe3+.
(3)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电.原因是Fe2+具有还原性.
(4)Ⅱ中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证.控制变量,做对照实验继续探究:电解pH=1的NaCl溶液,记录如表:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅳ | a>x≥c | 无明显变化 | 有Cl2 |
| Ⅴ | c>x≥b | 无明显变化 | 无Cl2 |
②Ⅳ中检验Cl2的实验方法:取少量阳极附近的溶液,滴在淀粉碘化钾试纸上,试纸变蓝色.
③与Ⅱ对比,得出的结论:通过控制电压,证实了产生Fe3+的两种原因都成立;通过控制电压,验证了放电顺序是:Fe2+>Cl-(填“>”或“<”)
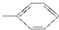 ⑤-CHO.
⑤-CHO.
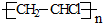 、I:
、I: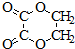 .
.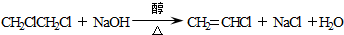 ;
; .
.