题目内容
【题目】(1)已知在2L的密闭容器中进行如下可逆反应,各物质的有关数据如下:
aA(g) |
| bB(g) |
| 2C(g) | |
起始物质的量浓度/(mol·L-1): | 1.5 | 1 | 0 | ||
2s末物质的量浓度/(mol·L-1): | 0.9 | 0.8 | 0.4 |
请回答下列问题。
①该可逆反应的化学方程式可表示为__。
②用物质B来表示0~2s的平均反应速率为__。
③从反应开始到2s末,A的转化率为__。
④下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是__(填序号)
A.vB(消耗)=vC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.vA:vB:vC=3:1:2
E.容器内气体C的物质的量分数保持不变
(2)①锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应方程式是2Zn+O2=2ZnO。则该电池的负极材料是__。
②瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池的示意图如图,该燃料电池工作时,电池的总反应方程式为__;负极的电极反应式为__。

【答案】3A(g)+B(g)![]() 2C(g) 0.1mol·L-1·s-1 40% BE 锌(或Zn) 4NH3+3O2=2N2+6H2O 2NH3-6e-+6OH-=N2+6H2O
2C(g) 0.1mol·L-1·s-1 40% BE 锌(或Zn) 4NH3+3O2=2N2+6H2O 2NH3-6e-+6OH-=N2+6H2O
【解析】
(1) 根据公式![]() 和表中数据可以求得
和表中数据可以求得![]() ①因为速率之比等于对应物质的化学计量数之比,所以
①因为速率之比等于对应物质的化学计量数之比,所以![]() ,
,![]() ,则
,则![]() ,
,![]() ,所以化学方程式为
,所以化学方程式为![]() ;故答案为:
;故答案为:![]() ;
;
②0~2s用物质B来表示的反应速率为![]() ,故答案为:0.1mol·L-1·s-1;
,故答案为:0.1mol·L-1·s-1;
③从反应开始到2s末,A物质的转化率![]() ,故答案为40%;
,故答案为40%;
④![]() (消耗)
(消耗)![]() (生成),正逆反应速率不相等,A项错误;该反应是反应前后气体体积不变的反应,容器内气体的总压强保持不变,说明各气体的物质的量不变,反应达到平衡状态,B项正确;容器内气体的密度始终不变,C项错误;只要反应发生,始终有
(生成),正逆反应速率不相等,A项错误;该反应是反应前后气体体积不变的反应,容器内气体的总压强保持不变,说明各气体的物质的量不变,反应达到平衡状态,B项正确;容器内气体的密度始终不变,C项错误;只要反应发生,始终有![]() ,D项错误;容器内气体C的物质的量分数保持不变,说明各组分的物质的量不变,反应达到平衡状态,E项正确,故答案选BE;
,D项错误;容器内气体C的物质的量分数保持不变,说明各组分的物质的量不变,反应达到平衡状态,E项正确,故答案选BE;
(2)①由反应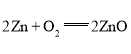 可知,锌失去电子,发生氧化反应,所以锌是负极,故答案为Zn(或锌);
可知,锌失去电子,发生氧化反应,所以锌是负极,故答案为Zn(或锌);
②在燃料电池的正极为氧气得到电子发生还原反应,碱性环境下的电极反应方程式为:O2+4e-+2H2O===4OH;负极上发生氨气失电子的氧化反应,电极反应式为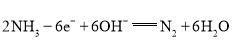 ,则电池的总反应相当于
,则电池的总反应相当于![]() 与
与![]() 反应生成
反应生成![]() 和
和![]() :
: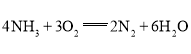 ;故答案为:4NH3+3O2=2N2+6H2O;2NH3-6e-+6OH-=N2+6H2O。
;故答案为:4NH3+3O2=2N2+6H2O;2NH3-6e-+6OH-=N2+6H2O。

【题目】I.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学们分别设计了如图甲、乙所示的实验装置。请回答相关问题:

(1)定性甲所示装置可通过观察___,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是___。
(2)定量如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为___,实验中需要测量的数据是___。
Ⅱ.以下是某研究小组探究影响反应速率部分因素的相关实验数据。
实验序号 | H2O2溶液浓度/% | H2O2溶液体积/mL | 温度/℃ | MnO2的用量/g | 收集O2的体积/mL | 反应所需时间/s |
① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
③ | 30 | 5 | 35 | 2 | 49.21 | |
④ | 30 | 5 | 55 | 2 | 10.76 |
(1)写出实验①中H2O2分解的化学方程式___。
(2)通过实验①和②对比可知,化学反应速率与____有关;从实验③和④对比可知,化学反应速率与温度的关系是___。