题目内容
【题目】原子序数小于36的X、Y、Z和铜四种元素,X的基态原子有3个不同的能级,有一个能级中的电子数比其它两个能级的中电子数都多1;Y基态原子中的电子占有5个轨道,其中有2个轨道处于半满状态,Z的原子序数为24。
(1)Z原子基态核外电子排布式为_____________。
(2)元素X与Y的第一电离能较大的__________________(填元素符号);H2Y2中Y原子轨道的杂化类型为__________。
(3)+3价Z的配合物K[Z(C2O4)2(H2O)2]中的配体是____________;与C2O42-互为等电子体的一种分子的化学式为_________。
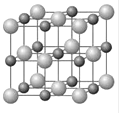
(4)Cu和Y形成的化合物的晶胞如图所示,晶胞中与铜离子距离相等且最近的铜离子有________个。某种有缺陷的铜和Y形成的化合物的晶体由Cu2+、Cu3+、Y2-及空隙组成,可表示为Cu0.98Y,则n(Cu2+)/n(Cu3+)=_________。
【答案】 1s22s22p63s23p63d54s1或[Ar]3d54s1 N sp3 H2O、C2O42- N2O4 12 47:2
【解析】试题分析:原子序数小于36的X、Y、Z和铜四种元素,X的基态原子有3个不同的能级,有一个能级中的电子数比其它两个能级的中电子数都多1,核外电子排布式为1s22s22p3,故X为N元素;Y基态原子中的电子占有5个轨道,其中有2个轨道处于半满状态,核外电子排布式为1s22s22p4,故Y为O元素;Z的原子序数为24,Z为Cr;
(1)Cr原子核外电子数为24,能量最低原理原理、洪特规则特例,核外电子排布式为:1s22s22p63s23p63d54s1;
(2)N元素原子2p能级为半满稳定状态,能量较低,第一电离能高于同周期相邻元素的,即N元素第一电离能高于O元素的;H2O2中O原子形成2个σ键,含有2对孤对电子,杂化轨道数目为4,O原子采取sp3杂化;
(3)+3价Cr的配合物K[Cr(C2O4)2(H2O)2]中的配体是H2O、C2O42-,与C2O42-互为等电子体的一种分子的化学式为:N2O4;
(4)晶胞中灰色球数目为4、黑色球数目为4,以顶点灰色球研究,与之距离最近的原子处于面心,每个顶点为8个晶胞共用,每个面心为2个晶胞共用,即晶胞中与铜离子距离相等且最近的铜离子有![]() ="12" 个,根据电荷守恒,则2n(Cu2+)+3n(Cu3+)=2,由原子守恒可知n(Cu2+)+n(Cu3+)=0.98,解得n(Cu2+)=0.94,n(Cu3+)=0.04,故n(Cu2+):n(Cu3+)=
="12" 个,根据电荷守恒,则2n(Cu2+)+3n(Cu3+)=2,由原子守恒可知n(Cu2+)+n(Cu3+)=0.98,解得n(Cu2+)=0.94,n(Cu3+)=0.04,故n(Cu2+):n(Cu3+)=![]() 。
。

 阅读快车系列答案
阅读快车系列答案【题目】A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B 在D中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1) A、B、D、E、F的原子半径由大到小排列的顺序为__________(用元素符号表示)
(2) 工业制备F单质的离子反应方程式为_________________。
(3) 由这些元素组成的物质,其组成和结构信息如下表:
物质 | 组成和结构信息 |
a | 含有A的二元离子化合物 |
b | 由D和E构成,且原子数之比为1:1 |
c | 化学组成EDF |
d | 只存在一种类型作用力且可导电的单质晶体 |
a的化学式 ;b的化学键类型 ;
c的一种作用 ;d的晶体类型 。
(4) 由A和B、D元素组成的两种二元化合物形成一类新能源物质。其中一种化合物分子通过 键构成具有空腔的固体;另一种化合物分子进入该空腔,形成可燃固体。