题目内容
如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cl- 离子核间距为a cm,氯化铯的摩尔质量为M g/mol,NA为阿伏加德罗常数,则氯化铯晶体的密度为( )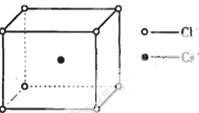
A. | B.   | C. | D. |
C
解析

 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案三氟化氮是一种无色、无味、无毒且不可燃的气体、在半导体加工,太阳能电池和液晶显示器的制造中得到广泛应用。NF3是一种三角锥形分子,键角102°,沸点-l29℃;可在铜的催化作用下由F2和过量NH3反应得到。
(1)写出制备NF3的化学反应方程式: 。
(2)NF3的沸点比NH3的沸点(-33℃)低得多的主要原因是 。
(3)与铜属于同一周期,且未成对电子数最多的元素基态原子核外电子排布式为 。
(4)理论上HF、NaAlO2和NaCl按6:1:2的物质的量之比恰好反应生成HCl、H2O和一种微溶于水的重要原料,该物质含有三种元素,在金属铝的冶炼中有重要作用。该物质为配合物,其中心离子是 ,配位数为 。
(5)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下面各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
①在周期表中,最可能处于同一族的是 和 。
②T元素最可能是 (填“s”“P” “d”或“ds”等)区元素,位于 族。若T为第2周期元素,F是第3周期元素中原子半径最小的元素,则T与F形成化合物的空间构型为 ,其中心原子的杂化方式为 。
下面有关晶体的叙述中,不正确的是( )
| A.金刚石为空间网状结构,由共价键形成的碳原子环上,最小的环上有6个碳原子 |
| B.氯化钠晶体中,每个Na+周围距离相等的Na+共有6个 |
| C.氯化铯晶体中,每个Cs+周围紧邻8个Cl- |
| D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子 |
科学家最近又发现了一种新能源——“可燃冰”。它的主要成分是甲烷分子的结晶水合物(CH4·nH2O)。其形成过程是:埋于海底地层深处的大量有机质在缺氧环境中,厌氧型细菌把有机质分解,最后形成石油和天然气,其中许多天然气被包进水分子中,在海底的低温与高压下形成了类似冰的透明晶体,这就是“可燃冰”。这种“可燃冰”的晶体类型是( )
| A.离子晶体 | B.分子晶体 | C.原子晶体 | D.金属晶体 |
石墨烯是由碳原子构成的单层片状结构的新材料(结构示意图如下),可由石墨剥离而成,具有极好的应用前景。下列说法正确的是( )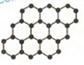
| A.石墨烯与石墨互为同位素 |
| B.0.12g石墨烯中含有6. 02×1022个碳原子 |
| C.石墨烯是一种有机物 |
| D.石墨烯中的碳原子间以共价键结合 |
下列各组物质的熔沸点按由低到高的顺序排列正确的是
| A.冰、干冰、氯化钠、金刚石 | B.汞、钠、烧碱、二氧化硅 |
| C.NaCl、KCl、CsCl | D.H2O、H2S、H2Se、H2Te |
据报道,国外科学家用激光将置于铁室中石墨靶上的碳原子炸松,再用射频电火花喷射
氮气,此时碳氮原子结合成碳氮化合物的薄膜,此化合物熔点比金刚石更高,其原因是( )
| A.碳氮化合物的分子间作用力大于金刚石 |
| B.氮原子最外层电子数比碳原子最外层电子数多 |
| C.碳、氮原子构成网状结构的晶体,碳氮键比金刚石中碳碳键更短 |
| D.碳、氮单质的化学性质均不活泼 |
氮化硅是一种新合成的超硬、耐磨、耐高温的材料。下列对氮化硅的叙述中,正确的是( )。
| A.氮化硅是分子晶体 |
| B.氮化硅是原子晶体 |
| C.氮化硅是离子晶体 |
| D.氮化硅化学式为Si4N3 |