题目内容
11.碱性电池具有容量大、放电电流大的特点,得到广泛应用.锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+MnO2(s)+H2O(l)═ZnO (s)+Mn(OH)2 (s),下列说法错误的是( )| A. | 电池工作时,锌失去电子 | |
| B. | 电池工作时,电子由正极通过外电路流向负极 | |
| C. | 电池正极的电极反应式为:MnO2(s)+2H2O(1)+2e-═Mn(OH)2 (s)+2OH-(aq) | |
| D. | 外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
分析 根据电池总反应式为:Zn(s)+MnO2(s)+H2O(l)═ZnO (s)+Mn(OH)2 (s),可知反应中Zn被氧化,为原电池的负极,负极反应为Zn-2e-+2OH-═ZnO+H2O,MnO2为原电池的正极,发生还原反应,正极反应为MnO2(s)+2H2O(1)+2e-═Mn(OH)2 (s)+2OH-(aq),以此解答该题.
解答 解:A、根据总反应可知Zn失去电子被氧化,为原电池的负极,故A正确;
B、原电池中,电子由负极经外电路流向正极,故B错误;
C、根据电池总反应式为:Zn(s)+MnO2(s)+H2O(l)═ZnO (s)+Mn(OH)2 (s),可知反应中Zn被氧化,为原电池的负极,负极反应为Zn-2e-+2OH-═ZnO+H2O,MnO2为原电池的正极,发生还原反应,正极反应为MnO2(s)+2H2O(1)+2e-═Mn(OH)2 (s)+2OH-(aq),故C正确;
D、负极反应为Zn-2e-+2OH-═Zn(OH)2,外电路中每通过O.2mol电子,消耗的Zn的物质的量为0.1mol,质量为0.1mol×65g/mol=6.5g,故D正确.
故选B.
点评 本题考查化学电源的工作原理,题目难度不大,注意电极反应方程式的书写和判断.

练习册系列答案
相关题目
2.下列物质中的主要成分不属于糖类的是( )
| A. | 棉花 | B. | 纤维素 | C. | 豆油 | D. | 淀粉 |
19.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 44g CO2含有氧原子数为NA | |
| B. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| C. | 23gNa在足量的O2中充分燃烧失去2mole-生成Na2O2 | |
| D. | 标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5 NA |
6.下列关于生活中常见药物的说法,不正确的是( )
| A. | “胃舒平”是治疗胃酸过多的药物 | |
| B. | “阿司匹林”是解热镇痛和消炎的药物 | |
| C. | “创可贴”是小伤口的外用消炎药物 | |
| D. | “风油精”是包治百病的药物 |
16.对于可逆反应mA+nB═pC+qD从正反应开始反应并在一定条件下达到平衡后,如果增大压强,则容器内气体平均相对分子质量增大,下列有关判断错误的是( )
| A. | 反应物A或B至少有一个是气体 | B. | 容器内不可能是单一气体 | ||
| C. | m+n可能大于p+q | D. | 若m<p,且D是气体,则B一定是气体 |
3.下列叙述正确的是( )
| A. | 氯化钠溶液在电流作用下电离成钠离子和氯离子 | |
| B. | 溶于水后能电离出氢离子的化合物一定是酸 | |
| C. | 硫酸钡难溶于水,故硫酸钡不属于电解质 | |
| D. | 二氧化碳溶于水能导电,但二氧化碳不属于电解质 |
1.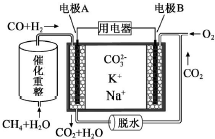 一种熔融碳酸盐燃料电池原理示意如图.下列有关该电池的说法正确的是( )
一种熔融碳酸盐燃料电池原理示意如图.下列有关该电池的说法正确的是( )
 一种熔融碳酸盐燃料电池原理示意如图.下列有关该电池的说法正确的是( )
一种熔融碳酸盐燃料电池原理示意如图.下列有关该电池的说法正确的是( )| A. | 如用此种电池电镀铜,待镀铜金属上增重19.2g,则至少消耗标准状况下2.24L CH4 | |
| B. | 电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O | |
| C. | 电池工作时,CO32-向电极B移动 | |
| D. | 电极B上发生的电极反应为:O2+2CO2+4e-=2CO32- |
 某校高一化学研究性学习小组对日常生活中的氯气用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等.
某校高一化学研究性学习小组对日常生活中的氯气用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等.