��Ŀ����
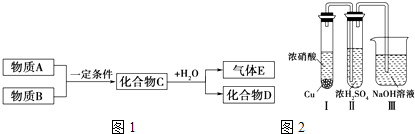
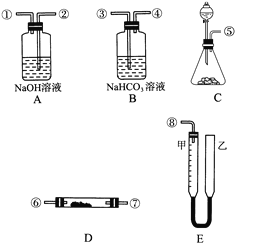
����Ŀ��ijѧ������С�飬ģ���������еķ�Ӧԭ�����������ͼ��ʾ����������ȡ���������������������ͼ������װ��E�ɼס���������������ɣ���������Ƥ����ͨ����װ������ˮ�����п̶�(0��50 mL)���������ã��ҹܿ������ƶ�����Һ��ߵ͡�ʵ��ɹ�ѡ�õ�ҩƷ���У�ϡ���ᡢ���ᡢ�������ơ�̼���ơ�����ʯ��ˮ��
�Իش�
(1)ͼ�и�װ�ýӿ�����˳����________(����ӿڵı�ţ��������ӽ��ܼ��г�װ�þ�ʡ��)��
(2)װ��C�з���ķ�Ӧ����________��________��
(3)װ��A��������______________��װ��B��������____________��
(4)Ϊ�˽�ȷ������������������˱���������װ�õ�������֮�⣬�ڶ���Ӧǰ�����Һ��Ķ����������ֵ�Ĺ����У�Ӧע��________��________��
a�������밼Һ����ʹ���ƽ
b���ȴ�Ƭ�̣����ҹ���Һ�治������ʱ���̶���
c������ǰӦ�����ƶ��ҹܣ�ʹ�ס�������Һ����ƽ
d������ʱ��һ��ʹ�ס�������Һ����ƽ
���𰸡�(1)�ݢۢܢޢߢڢ٢�(�ޢ߿ɻ�λ)
(2)����ʯ ����
(3)��ȥ����O2��δ��Ӧ��CO2 ����CO2�л��е�HCl
(4)a c
��������װ��C�в�����CO2���壬��ͨ��NaHCO3��Һ��ȥ���л��е�HCl���壬CO2������Na2O2���巴Ӧ�������O2�в��ɱ���ػ���CO2���壬����ͨ��NaOH��Һ��ȥ�����У�ϴ��װ���������ķ���ע��ӦΪ���ܽ����̹ܳ���ͬʱ��Ϊȷ��������O2��������ڷ�Ӧǰ���ȡ����Һ��Ķ���ʱ��Ӧ�����ƶ��ҹܣ�ʹ�ס�������Һ����ƽ���Ա�֤��Һ���Ϸ�Ϊ1������ѹ������ʱ����Ӧ�밼Һ����ʹ���ƽ��

����Ŀ����Ҫ�����
��1����ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̣���ѧ���ļ������γɣ����1mol��ѧ��ʱ�ͷţ������գ�����������֪��N��N���ļ�����948.9kJmol��1 �� H��H���ļ�����436.0kJmol��1����N2��H2�ϳ�1mol NH3ʱ�ɷų�46.2kJ��������N��H���ļ�����
��2����������������Ӧ����1molˮ����������241.8KJ��д���÷�Ӧ���Ȼ�ѧ����ʽ���� ��
��֪������NO��O2��Ӧ����1molNO2���ʱ�Ϊ��57.07KJ��1molNO2��H2O��Ӧ����HNO3��Һ��NO���ʱ�Ϊ��46KJ��д��NO��O2��ˮ����HNO3��Һ���Ȼ�ѧ����ʽ�� ��
��3��ij�¶��´�ˮ�е�c��H+��=2��10��7mol/L�����ʱc��OH����=mol/L���ô�ˮ��pH�����7��������7������=7���������¶Ȳ��䣬����ϡ����ʹc��H+��=5��10��6mol/L����c��OH����=mol/��
��4������MgO�������������Ȼ�þ�ϳɣ�ijС���о��÷�Ӧ���¶�Ϊ378��398Kʱ�ķ�Ӧʱ�䡢��Ӧ����ȵ����ض�����ʵ�Ӱ�죮���������ʵ����Ʊ���
��� | �¶�/K | ��Ӧʱ��/h | ��Ӧ�����ʵ������ | ʵ��Ŀ�� |
�� | 378 | 3 | 3��1 | ʵ��ں͢�̽�� |
�� | 378 | 4 | 4��1 | |
�� | 378 | 3 | ||
�� | 398 | 4 | 4��1 |
����Ŀ����ͼ����0.1000mol/L������ζ�ijδ֪Ũ�ȵ�NaOH��Һ��ʾ��ͼ��ij�εζ�ǰ�����ʢ������ζ�����Һ���λ�ã���ش� 
��1������A����������
��2����������������
�ζ�ǰ����ΪmL��
�ζ������ΪmL��
��3��ijʵ��С��ͬѧ������ʵ���ʵ���������±���ʾ�� ���ݱ������ݼ�����Ĵ���NaOH��Һ��ƽ��Ũ����mol/L����������λ��Ч���֣�
ʵ�� | ����NaOH��Һ�������mL�� | �ζ�ǰ����� | �ζ�������� |
1 | 20.00 | 1.20 | 23.22 |
2 | 20.00 | 2.21 | 24.21 |
3 | 20.00 | 1.50 | 23.48 |
��4�����÷�̪��ָʾ�����жϵ���ζ��յ��ʵ��������
��5�������м��ּٶ�����������ۣ������Ӱ�족����ƫ�ߡ�����ƫ�͡���
�����ζ�ǰ��ƿδ�ô���Һ��ϴ���Բⶨ�����Ӱ������
��ȡ����Һ�ĵζ��ܣ��ζ�ǰ�ζ��ܼ�������ݣ��ζ���������ʧ��
�۱�Һ����ʱ�����ζ�ǰ���ӣ��ζ����ӣ��Բⶨ�����Ӱ���� ��