题目内容
(14分)合成氨是人类科学技术发展史上的一项重大突破。合成氨反应的化学方程式为N2(g)+3H2(g)≒2NH3(g)。一定条件下,在密闭容器中反应达平衡后,请回答:
(1)若增大N2的浓度,则化学反应速率 (填“增大”或“减小”),化学平衡
(填“向正反应方向”、 “向逆反应方向”或“不”)移动,N2的转化率_________。
“向逆反应方向”或“不”)移动,N2的转化率_________。
(2)若加入适当的催化剂,则化学反应速率增大,化学平衡 (填“向正反应方向”、“向逆反应方向”或“不”)移动。
(3)若减压时,N2的质量分数_________。(填“增大”“减小”或“不变”,)
(4)从化学平衡移动的角度分析,提高H2转化率可以采取的措施是 (选填序号字母)。
(选填序号字母)。
a、及时分离出NH3 b、升高温度 c、增大压强 d、使用催化剂
(5)写出该反应的化学平衡常数表达式:K= 。
(1)若增大N2的浓度,则化学反应速率 (填“增大”或“减小”),化学平衡
(填“向正反应方向”、
 “向逆反应方向”或“不”)移动,N2的转化率_________。
“向逆反应方向”或“不”)移动,N2的转化率_________。(2)若加入适当的催化剂,则化学反应速率增大,化学平衡 (填“向正反应方向”、“向逆反应方向”或“不”)移动。
(3)若减压时,N2的质量分数_________。(填“增大”“减小”或“不变”,)
(4)从化学平衡移动的角度分析,提高H2转化率可以采取的措施是
 (选填序号字母)。
(选填序号字母)。 a、及时分离出NH3 b、升高温度 c、增大压强 d、使用催化剂
(5)写出该反应的化学平衡常数表达式:K= 。

略

练习册系列答案
相关题目
 CO(气)+H2(气)在一可变容积的闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
CO(气)+H2(气)在一可变容积的闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
 对该反应不影响。
对该反应不影响。 出主要实验步骤。
出主要实验步骤。 2NH3(g),增大氮气浓度可增加活化分子百分数,从而使反应速率增大
2NH3(g),增大氮气浓度可增加活化分子百分数,从而使反应速率增大
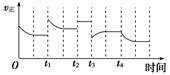
 2NH3(g) ΔH=-92.4 kJ·mol-1,在反应过程中,正反应速率的变化如下图: 下列说法正确的是( )
2NH3(g) ΔH=-92.4 kJ·mol-1,在反应过程中,正反应速率的变化如下图: 下列说法正确的是( )