题目内容
【题目】某有机物由C、H、O三种元素组成。取8.88g样品在如下装置中用电炉加热充分燃烧,通过测定生成的CO2和H2O的质量,再借助质谱图确定其分子式。
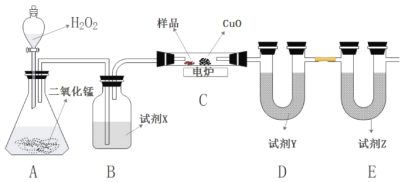
请回答下列问题:
(1)B装置中试剂X为____________。
(2)D装置中试剂Y为_______(填“无水氯化钙”或“碱石灰”下同),E装置中试剂Z为_________。
(3)如果C装置中没有CuO,碱石灰装置的增重将____________(填“增大”“减”或“不变”下同)。
(4)实验测得无水氯化钙装置增重10.8g;碱石灰裝置增重21.12g,由质谱仪测得该有机物的相对分子量为74,则该有机物的分子式为___。
(5)该有机物红外光谱图上有羟基的强吸收峰,试写出该有机物可能的结构简式________________。
【答案】浓硫酸 无水氯化钙 碱石灰 减小 C4H10O CH3CH2CH2CH2OH、CH3CH2CH(OH)CH3、(CH3)2CHCH2OH、(CH3)3COH
【解析】
在装置A中,H2O2在MnO2的催化作用下分解生成O2;在B装置中浓硫酸的作用下干燥O2;在C装置中CuO的作用下样品燃烧生成CO2和H2O,依题意知,装置D中无水氯化钙吸收水蒸气,在装置E中碱石灰吸收CO2。
(1)依据分析可知,B装置应为O2的干燥装置,所以加入试剂X为浓硫酸。答案为:浓硫酸;
(2)因为碱石灰可同时吸收CO2和水蒸气,而D装置的作用是只吸收水蒸气,所以试剂Y为无水氯化钙,E装置中试剂Z为碱石灰。答案为:无水氯化钙;碱石灰;
(3)如果C装置中没有CuO,有机物中的碳元素可能有一部分没有转化为CO2,从而导致碱石灰装置的增重将减小。答案为:减小;
(4)无水氯化钙吸收水的质量为10.8g;碱石灰吸收CO2的质量为21.12g,有机物的相对分子量为74,n(有机物)=![]() =0.12mol,n(CO2)=
=0.12mol,n(CO2)=![]() =0.48mol,n(H2)=
=0.48mol,n(H2)=![]() =0.6mol,则1mol有机物燃烧生成4molCO2和5molH2O,有机物分子中含氧原子数
=0.6mol,则1mol有机物燃烧生成4molCO2和5molH2O,有机物分子中含氧原子数![]() =1,该有机物的分子式为C4H10O。答案为:C4H10O;
=1,该有机物的分子式为C4H10O。答案为:C4H10O;
(5)该有机物红外光谱图上有羟基的强吸收峰,则表明有机物分子中含有1个醇羟基,试该有机物可能的结构简式为CH3CH2CH2CH2OH、CH3CH2CH(OH)CH3、(CH3)2CHCH2OH、(CH3)3COH。答案为:CH3CH2CH2CH2OH、CH3CH2CH(OH)CH3、(CH3)2CHCH2OH、(CH3)3COH。

 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案【题目】下列实验不能达到预期目的的是
选项 | 实验操作 | 预期目的 |
A | 充满NO2的密闭玻璃球分别浸泡在冷、热水中 | 研究温度对化学平衡移动的影响 |
B | 向盛有 1 mL 硝酸银溶液的试管中滴加 NaCl 溶液至不再有沉淀产生,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种更难溶的沉淀 |
C | 苯酚和水的浊液中,加稍过量浓碳酸钠溶液 | 比较苯酚与碳酸的酸性 |
D | 向2支试管中加入同体积同浓度H2C2O4溶液, 再分别加入同体积不同浓度的酸性KMnO4溶液 | 依据褪色时间来研究浓度对反应速率的影响 |
A.AB.BC.CD.D