题目内容
【题目】有一化学反应aA+bB=C,根据影响化学反应速率的因素可得v(C)=kcm(A)cn(B)。其中k是与温度有关的常数,为测k、m、n的值,在298 K时,将A、B溶液按不同的浓度混合,得到下列实验数据:
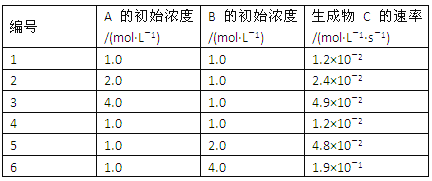
(1)根据上表可求得:m=_______,n=______,k=________。
(2) 当c(A)=c(B)=2.0mol/L时,用B表示的初始反应速率为___________________。
【答案】1 21.2×10-20.192 mol/(L·s)
【解析】
(1)将表1、2数据带入v(C)=kcm(A)cn(B),可得v2/v1=2m=2, m=1;将表1、3数据带入v(C)=kcm(A)cn(B),可得v3/v1=2n=4, n=2;将m=1,n=2及数据1代入v(C)=kcm(A)cn(B)可得:k×11×12=1.2×102,解得K= 1.2×10-2,正确答案:1;2 ;1.2×10-2 。
(2)当c(A)=c(B)=2.0mol/L时,根据v(C)=kcm(A)cn(B),v(C)=1.2×10-2×21×22=9.6×10-2,因为m=1,n=2,所以aA+bB=C反应中,a=1,b=2,根据速率之比和系数成正比规律可知:v(B)=2 v(C)=2×9.6×10-2=0.192 mol/(L·s);正确答案:0.192 mol/(L·s)。

【题目】t℃时,在体积不变的容器中发生反应X(g)+3Y(g) ![]() 2Z(g) △H<0,各组分浓度如下表,下列说法不正确的是
2Z(g) △H<0,各组分浓度如下表,下列说法不正确的是
物质 | X | Y | Z |
初始浓度/ mol·L-1 | 0.1 | 0.3 | 0 |
2min末浓度/mol·L-1 | 0.08 | ||
平衡浓度/mol·L-1 | 0.1 |
A. 0~2min的平均速率ν(X) =0. 01 mol·L-1·min-1
B. 达平衡时Y的转化率为50%
C. 其它条件不变,升高温度,平衡逆向移动
D. 其它条件不变,增加X的浓度,ν正增大、ν逆减小,平衡正向移动