题目内容
用5mol/L的氯化钠溶液配制0.1mol/L的氯化钠溶液500mL,无需使用到的仪器是( )
| A.托盘天平 | B.量筒 | C.500mL容量瓶 | D.胶头滴管 |
A
解析试题分析:实验操作的步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,并用玻璃棒搅拌,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯和玻璃棒2~3次,并将洗涤液移入容量瓶中,继续当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加水到凹液面与刻度线水平相切,盖好瓶塞,反复颠倒上下摇匀,移入试剂瓶贴标签贮存.所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管.量筒可用可不用.选A.
考点:配制一定物质的量浓度的溶液

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列叙述中正确的是
| A.1mol氯气参加氧化还原反应,转移的电子数一定为2NA |
| B.在同温同压下,相同体积的任何气体单质所含的原子数目相同 |
| C.14 g乙烯和丙烯的混合物中总原子数为3NA个 |
| D.含2molH2SO4的浓硫酸与足量铜片在加热条件下反应,一定能产生NA个SO2气体分子 |
设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,2.24 L水中所含电子总数为NA |
| B.1 L 0.2 mol·L-1硫酸铁溶液中含有的SO42-数为0.2NA |
| C.苯和苯甲酸混合物1 mol,完全燃烧消耗O2的分子数为7.5NA |
| D.标准状况下,7.1 g氯气与足量石灰乳充分反应转移电子数为0.2NA |
a g Fe2O3和Al2O3组成的混合物全部溶于20mL、物质的量浓度为0.05mol/L的硫酸中,反应后向所得溶液中加入10mLNaOH溶液,恰好使Fe3+、Al3+完全沉淀,则氢氧化钠溶液的物质的量浓度为
| A.0.1mol/L | B.0.2 mol/L | C.0.4mol/L | D.0.8mol/L |
NA表示阿伏加德罗常数,以下各物质所含分子数最多的是( )
| A.标准状况下11.2 L氯气 | B.17g氨气 |
| C.0.8mol氧气 | D.4℃时,36mL的H2O |
下列与阿伏加德罗常数的值(NA)有关的说法正确的是( )
| A.NA个Fe(OH)3胶体粒子的质量为107g |
| B.8.0 gCu2S和CuO的混合物中含有铜原子数为0.1NA |
| C.标准状况下,2.24 L Cl2溶于水中达到饱和,可得到HClO分子的数目是0.1NA |
| D.2.3gNa与氧气完全反应,反应中转移的电子数介于0.1 NA到0.2 NA之间 |
用NA表示阿伏伽德罗常数的值,下列叙述不正确的是
| A.18g重水含有10NA中子 | B.10.6gNa2CO3固体有0.1NAC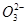 |
| C.6.4gCu失去的电子数可能为0.1NA | D.1mo1H2C2O4能消耗2NAOH— |
下列叙述正确的是
| A.3.01×1023个SO2分子的质量为32g |
| B.CH4的摩尔质量为16g |
| C.1 mol H2O的质量为18g/mol |
| D.标准状况下,1 mol任何物质体积均为22.4L |
用1L1mol·L-1NaOH溶液吸收0.8molCO2,所得溶液中Na2CO3和NaHCO3的物质的量之比约为( )
| A.1︰3 | B.1︰2 | C.2︰3 | D.3︰2 |