题目内容
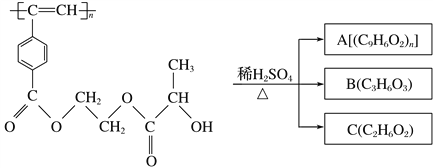
【题目】Ⅰ.在有机化学分析中,根据反应的性质和反应产物,即可确定烯烃的组成和结构(双键及支链的位置),例如: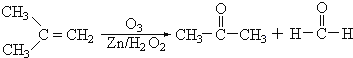
据以上线索和下列反应事实,确定C7H14的结构和名称:
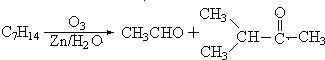
(1)该烃的结构简式是_______________________________。
(2)名称是_______________________________。
Ⅱ.把不饱和烃在催化剂存在下用O3氧化则生成有羰基的化合物,其规律可用下式表示:![]() 。现把一定量的以分子式为C4H8的不饱和烃的混合体。用上述方法进行氧化,生成0.5mol酮,1.5mol醛,其中含甲醛0.7mol,另外把1.0mol混合气体进行加氢反应,生成1.0mol饱和烃的混合气体。则上述混合气体经臭氧氧化后 可生成的物质:(用结构简式表示):_________________。
。现把一定量的以分子式为C4H8的不饱和烃的混合体。用上述方法进行氧化,生成0.5mol酮,1.5mol醛,其中含甲醛0.7mol,另外把1.0mol混合气体进行加氢反应,生成1.0mol饱和烃的混合气体。则上述混合气体经臭氧氧化后 可生成的物质:(用结构简式表示):_________________。
【答案】 (CH3)2CHC(CH3)=CHCH3 3,4--二甲基-2-戊烯 ![]()
【解析】Ⅰ.(1)由题中信息可知,只要把氧化后的产物中的2个羰基碳原子用双键连接,即可得到氧化前的物质,所以该烃的结构简式是(CH3)2CHC(CH3)=CHCH3。
(2)名称是3,4--二甲基-2-戊烯。
Ⅱ.分子式为C4H8的不饱和烃有1-丁烯、2-丁烯和2-甲基丙烯等3种,经臭氧化后,1-丁烯可生成甲醛和丙醛,2-丁烯可生成乙醛,2-甲基丙烯可生成甲醛和丙酮。根据C4H8的实际氧化产物为0.5mol酮、1.5mol醛,其中含甲醛0.7mol,可以判断原来有0.5mol 2-甲基丙烯、0.2mol 1-丁烯、0.3mol 2-丁烯。因此,生成物中除甲醛外,还有乙醛、丙醛和丙酮,其结构简式为:![]() 。
。

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案【题目】硫酸年产量的高低可衡量一个国家化工生产水平发展的高低,SO2转化为SO3是制备硫酸中的关键性反应,也是一个可逆反应。
(1)NO可作为SO2与O2间反应的催化剂,催化机理如下:
①2NO(g)+O2(g)![]() 2NO2(g)ΔH1=-113kJ/mol
2NO2(g)ΔH1=-113kJ/mol
②SO2(g)+NO2(g)![]() SO3(g)+NO(g) ΔH2
SO3(g)+NO(g) ΔH2
总反应:2SO2(g)+O2(g)![]() 2SO3(g)ΔH3=-196.6kJ/mol ΔH2=__________
2SO3(g)ΔH3=-196.6kJ/mol ΔH2=__________
(2)一定温度下,向容积为2L的恒容密闭容器中充入2molSO2、2mo1O2测得容器中压强的变化如下表所示(SO3为气体):
反应时间/min | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
压强/MPa | 16.0a | 14.7a | 13.7a | 13.0a | 12.5a | 12.4a | 12.4a |
①0~10min内,υ(SO2)=_________
②该温度下的平衡常数K=__(结果保留一位小数)。
③反应达到平衡后,再向容器中同时充入均为0.2mol的三种气体后,υ(正)、υ(逆)的关系是___
(3)一定温度下,向某密闭容器中通入一定量的二氧化硫和氧气的混合气体并使之反应,反应过程中SO2、O2、SO3物质的量变化如下图所示:
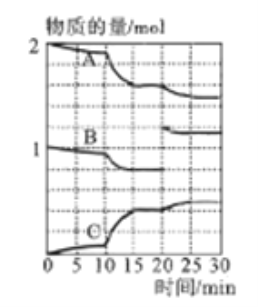
①A、B、C三条曲线中表示SO2物质的量的变化的是__,若在15~20min、25~30min两个时间段内容器容积不变,则在某一时刻SO3的分解速率较大的时间段是_______。
②10~15min内反应速率发生了明显变化,其可以的原因有__________
(4)常温下,用NaOH溶液吸收SO2既可消除SO2造成的大气污染,也可获得重要的化工产品,若某吸收液中c(HSO3-):c(SO32-)=1:100,则所得溶液的pH=______(常温下K1(H2SO3)=1.5×10-2、K2(H2SO3)=1×10-7