题目内容
硫酸、硝酸和盐酸既是重要的化工原料也是化学实验室里必备的试剂。
(1)常温下,可用铝槽车装运浓硫酸,这是因为浓硫酸具有 性;硝酸应保存在棕色试剂瓶中,这是因为硝酸具有 性;敞口放置的浓盐酸浓度会减小,这是因为盐酸具有 性。
(2)①在100 mL 18 mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积为13.44 L,则参加反应的铜片的质量为 (选填序号);
a.115.2 g b.76.8 g c.57.6 g d.38.4 g
②若使上述①中反应剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式: 。
(3)工业制盐酸是以电解饱和氯化钠溶液为基础进行的,该电解过程中阳极的电极反应式为: 。
(1)(3分)强氧化 不稳定 挥发
(2)(3分)d(1分) 3Cu + 8H+ + 2NO3—=3Cu2+ + 2NO↑+ 4H2O(2分)
(3)(2分)2Cl— — 2e—=Cl2↑
解析试题分析:(1)由于浓硫酸具有强氧化性,在常温下能使铝发生钝化,所以常温下,可用铝槽车装运浓硫酸;浓硝酸见光易分解生成NO2、氧气和水,所以硝酸应保存在棕色试剂瓶中;由于浓盐酸易挥发,所以敞口放置的浓盐酸浓度会减小。
(2)①标准状况下13.44L气体的物质的量=13.44L÷22.4L/mol=0.6mol,根据方程式2H2SO4(浓)+Cu  CuSO4+2H2O+SO2↑可知,参加反应的铜的物质的量是0.6mol,质量=0.6mol×64g/mol=38.4g,答案选d。
CuSO4+2H2O+SO2↑可知,参加反应的铜的物质的量是0.6mol,质量=0.6mol×64g/mol=38.4g,答案选d。
②由于随着反应的进行,浓硫酸的浓度逐渐降低。而铜与稀硫酸不反应,因此反应中硫酸过量。又因为在酸性条件下硝酸盐具有强氧化性,因此能氧化剩余的铜,反应的离子方程式为3Cu + 8H+ + 2NO3—=3Cu2+ + 2NO↑+ 4H2O。
(3)电解池中阳极失去电子,发生氧化反应。因此惰性电极电解饱和食盐水时阳极是氯离子放电,电极反应式为2Cl— — 2e—=Cl2↑。
考点:考查浓硫酸、浓硝酸和浓盐酸的性质;氧化还原反应的有关判断和计算;电极反应式的书写

 阅读快车系列答案
阅读快车系列答案光纤预制棒是光缆生产的最“源头”项目,目前国内光缆生产厂家约200家,大部分靠买进口光纤预制棒来生产光缆。
(1)光纤预制棒跟光导纤维的成分相同,那么光纤预制棒的化学成分是 。
(2)如果把光缆裸露在碱性土壤中,结果会短路,用离子方程式说明原因 。
(3)下列说法正确的是 。
| A.石英与普通玻璃都是硅酸盐制品 |
| B.二氧化硅是良好的半导体材料 |
| C.工艺师用盐酸刻蚀石英制作艺术品 |
| D.石英与二氧化碳中的化学键相同 |
盐酸、硫酸和硝酸都是重要的化工原料,也是化学实验室里必备的重要试剂。请回答下列问题:
(1) 常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有 性,用玻璃棒蘸取浓硫酸滴在纸上,纸逐渐变黑,说明浓硫酸具有 性,实验室不能用浓硫酸干燥氨气,说明硫酸具有 性。
(2) 硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,工业上用洗净的废铜屑作原料来制备硝酸铜。右图所示制备方法符合“绿色化学”思想的
是 (填序号)。
(3) ①在100ml 18 mol/L浓硫酸中加入过量铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是 。
| A.40.32 L | B.30.24 L | C.20.16 L | D.13.44 L |
(4) 某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水,则反应的化学方程式为 。




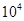 L(标准状况)该尾气需42.5gNH3,则x= _ 。
L(标准状况)该尾气需42.5gNH3,则x= _ 。

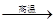 Si3N4 +12HCl
Si3N4 +12HCl