��Ŀ����
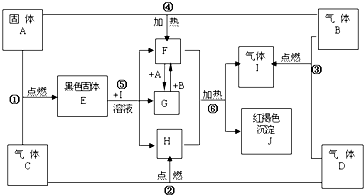
����A��B��C��D��E��F��G��H��I��J����ͼ��ʾ��ת����ϵ��

ͼ���������ʾ��ɶ�����Ԫ����ɣ���ÿ��С�������ڵ��������ʾ����ٺ��е��������е�һ����ͬԪ�ء�������Ϣ���±���
|
��� |
�� Ϣ |
|
1 |
DΪ�ؿ��к�����ߵ�Ԫ����ɵĵ��� |
|
2 |
EΪ������̬������ |
|
3 |
F��Ũ��Һ��������� |
|
4 |
HΪ����ɫ���廯���� |
|
5 |
��ⱥ��J��Һ�ǹ�ҵ��Ҫ��Ӧ |
|
6 |
CΪ���ӻ�������������Ӿ����н���Ԫ�� |
��1��д��G�Ļ�ѧʽ�� ��ָ��H�л�ѧ�������ͣ� ��
��2�������²��һ��Ũ�ȵ�C��Һ��pH=10�������ӷ���ʽ��ʾ��ԭ�� ��
��3��д����H��Է���������ͬ�������ǵ������������ĵ������������Ҳ����ͬ�Ļ�����Ļ�ѧʽ ��
��4��д��C��Һ��ͨ�����CO2�Ļ�ѧ����ʽ�� ��

��5��ͨ��һ��Ũ�ȵĿ��Լ���Һ�У�����ǡ����ȫ��Ӧ����֪��Ӧ���̷��ȣ��������������ֺ�YԪ�ص����ӣ����������������ʵ�����n���뷴Ӧʱ�䣨t���ı仯ʾ��ͼ����ͼ��ʾ��д���÷�Ӧ�����ӷ���ʽ�� ���ÿ��Լ���Һ��KOH�������� g��
��1����4�֣�SO3��H2SO4 ��2�֣����Ӽ������ۼ���2�֣�
��2����4�֣�AlO2-+2H2O = Al(OH)3+OH‾ (��Al(OH)4- + CO2 = Al(OH)3+OH‾
��3����2�֣�Na2S
��4����2�֣�CO2+ NaAlO2 +2H2O = NaHCO3 + Al(OH)3��(��Na[Al(OH)4] + CO2 = NaHCO3 + Al(OH)3��
��5����4�֣�5Cl2 + 10OH‾ = 2ClO‾ + ClO3‾ + 7Cl‾ + 5H2O��2�֣���16.8��2�֣�
��������
������������������Ŀ������Ϣ��ͼ���������ʾ��ɶ�����Ԫ����ɣ���ÿ��С�������ڵ��������ʾ����ٺ��е��������е�һ����ͬԪ�ء���1����ΪEΪ������̬���������EΪSO2 ��SO3 ����GΪSO3 ��H2SO4 ��HΪ����ɫ���廯����ΪNa2O2 �������Ӽ������ۼ���
��2��CΪ���ӻ�������������Ӿ����н���Ԫ�أ�ΪNaAlO2������Һ�Լ�������ΪAlO2-������ˮ�ⷴӦ��
��3��Na2O2 ��O22‾��S2‾���������������ͬ�����Ը�����ΪNa2S ��
��4����NaAlO2��Һ��ͨ�����CO2 ����NaHCO3�� Al(OH)3��