题目内容
(7分)二氧化锰是制造锌锰干电池的基本材料.工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下:
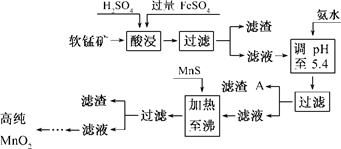
某软锰矿的主要成分为MnO2,还含Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为______________________________.
(2)滤渣A的主要成分为________.
(3)加入MnS的目的是除去________杂质.
(4)碱性锌锰干电池中,MnO2参与的电极反应方程式为__________________________.
(5)从废旧碱性锌锰干电池中可以回收利用的物质有________(写出两种).

某软锰矿的主要成分为MnO2,还含Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
| 沉淀物 | pH |
| Al(OH)3 | 5.2 |
| Fe(OH)3 | 3.2 |
| Fe(OH)2 | 9.7 |
| Mn(OH)2 | 10.4 |
| Cu(OH)2 | 6.7 |
| Zn(OH)2 | 8.0 |
| CuS | ≥-0.42 |
| ZnS | ≥2.5 |
| MnS | ≥7 |
| FeS | ≥7 |
(2)滤渣A的主要成分为________.
(3)加入MnS的目的是除去________杂质.
(4)碱性锌锰干电池中,MnO2参与的电极反应方程式为__________________________.
(5)从废旧碱性锌锰干电池中可以回收利用的物质有________(写出两种).
(1)MnO2+2FeSO4+2H2SO4===MnSO4+Fe2(SO4)3+2H2O
(2)Fe(OH)3、Al(OH)3 (3)Cu2+、Zn2+
(4)MnO2+H2O+e-===MnOOH+OH- (5)Zn、MnO2
(2)Fe(OH)3、Al(OH)3 (3)Cu2+、Zn2+
(4)MnO2+H2O+e-===MnOOH+OH- (5)Zn、MnO2
(1)根据FeSO4在反应条件下将MnO2还原为MnSO4,Fe2+被氧化为Fe3+,可以写其反应方程式2FeSO4+MnO2+2H2SO4===MnSO4+Fe2(SO4)3+2H2O。
(2)根据反应后滤液(Mn2+、Fe3+、Al3+、Cu2+、Zn2+、Fe2+)加氨水调pH至5.4,结合题表可知滤渣A的主要成分为Fe(OH)3和Al(OH)3。
(3)根据题表可知加入MnS是为了生成溶解度更小的CuS、ZnS而除去Cu2+、Zn2+.
(4)碱性锌锰干电池中Zn作负极,则MnO2作正极得电子.其电极反应式应为 MnO2+H2O+e-===MnOOH+OH-。
(5)从碱性锌锰干电池的原料可知,其废旧电池可回收利用的物质为锌和MnO2。
(2)根据反应后滤液(Mn2+、Fe3+、Al3+、Cu2+、Zn2+、Fe2+)加氨水调pH至5.4,结合题表可知滤渣A的主要成分为Fe(OH)3和Al(OH)3。
(3)根据题表可知加入MnS是为了生成溶解度更小的CuS、ZnS而除去Cu2+、Zn2+.
(4)碱性锌锰干电池中Zn作负极,则MnO2作正极得电子.其电极反应式应为 MnO2+H2O+e-===MnOOH+OH-。
(5)从碱性锌锰干电池的原料可知,其废旧电池可回收利用的物质为锌和MnO2。

练习册系列答案
相关题目
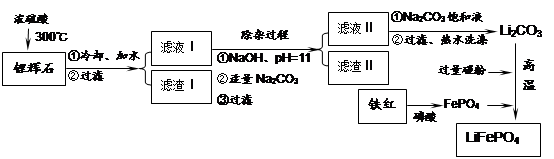
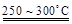 Li2SO4 + Al2O3·4SiO2·H2O↓
Li2SO4 + Al2O3·4SiO2·H2O↓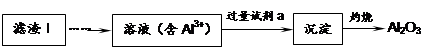
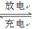 LiFePO4,电池中的固体电解质可传导Li+。试写出该电池放电时的正极反应: 。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为 。
LiFePO4,电池中的固体电解质可传导Li+。试写出该电池放电时的正极反应: 。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为 。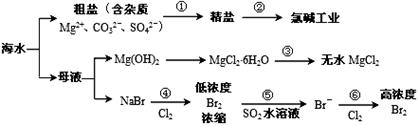
 4Al+3O2↑
4Al+3O2↑ 2Fe+3CO2
2Fe+3CO2 2Na+Cl2↑
2Na+Cl2↑ 请回答氯碱工业的如下问题:
请回答氯碱工业的如下问题: