题目内容
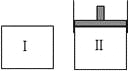
【题目】短周期元素X、Y、Z、W在元素周期表中的位置关系如图。若Y原子的最外层电子数是内层电子数的3倍,则下列说法正确的是

A. 原子半径: W>Z>Y>X
B. 四种元素的单质中,Z单质的熔沸点最高
C. 最高价氧化物对应水化物的酸性:Z>W>X
D. Z的氢化物的稳定性大于W的氢化物
【答案】B
【解析】X、Y、Z、W均为短周期元素,根据元素在周期表中的位置知,X、Y为第二周期元素,Z和W属于第三周期元素,Y原子的最外层电子数是内层电子数的3倍,则Y是O元素,根据其位置知X是N元素、Z是S元素、W是Cl元素。A.原子电子层数越多,其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小,所以原子半径大小顺序是Z>W>X>Y,故A错误;B.四种元素对应的单质中,常温下S为固体,而其它3种都是气体,所以Z(S元素)对应的单质熔沸点最高,故B正确;C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性W>Z,所以其最高价氧化物的水化物酸性W>Z,故C错误;D. 元素的非金属性越强,氢化物越稳定,非金属性W>Z,Z的氢化物的稳定性小于W的氢化物,故D错误;故选B。

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
【题目】近年来科学家制造出大量的新物质,对下列三种物质的相关说法错误的是( )
|
|
|
石墨烯:从石墨中分离出来,是最薄、最坚硬的纳米材料 | 石墨炔:平面网状结构的全碳分子,具有优良的化学稳定性 | 纳米碳管:具有优良的场发射性能,制作成阴极显示管、储氢材料 |
A. 石墨烯具有良好的导电性
B. 上述三种物质与金刚石互为同素异形体
C. 石墨炔孔径略大于H2分子的直径,可作H2的提纯薄膜
D. 上述三种物质与浓硫酸都能发生反应,但反应产物不同