题目内容
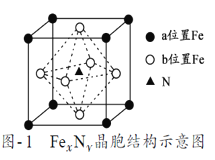
【题目】肼(N2H4)分子中所有原子均达到稀有气体原子的稳定结构,它的沸点高达113℃,已知肼的球棍模型如图所示,下列有关说法不正确的是
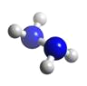
A. 肼是由极性键和非极性键构成的非极性分子
B. 肼沸点高达113℃,可推测肼分子间能形成氢键
C. 肼分子中N原子采用sp2杂化方式
D. 32g肼分子中含有5NA个σ键
【答案】C
【解析】
A、肼分子中含有极性键和非极性键,正负电荷重心重合,为非极性分子,故A正确;
B、肼中含有N-H键,分子间能形成氢键,沸点较高,故B正确;
C、肼的结构简式是H2N-NH2,每个氨基的中心原子氮都采用sp3杂化,故C错误;
D、32g肼的物质的量为n=32g/32g.mol=1mol,1mol肼中含5molσ键,含有σ键的总数为5NA,故D正确。
正确答案选C。

练习册系列答案
相关题目