题目内容
【题目】著名的获得诺贝尔奖的狄尔斯![]() 阿德尔反应,是由共轭双烯与烯烃或炔烃反应生成六元环的反应。如:CH2=CH-CH=CH2+CH2=CH2
阿德尔反应,是由共轭双烯与烯烃或炔烃反应生成六元环的反应。如:CH2=CH-CH=CH2+CH2=CH2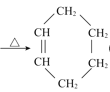
![]() 可表示为
可表示为![]()
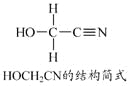
![]() ,实际是个加成反应。工业上常用下列流程制取重要化学原料
,实际是个加成反应。工业上常用下列流程制取重要化学原料![]() (M)。
(M)。

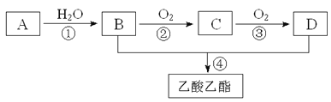
流程中的A为天然橡胶的单体,分子式为C5H8。
(1)A的名称是___,B的结构简式是___。
(2)A的属于炔烃的同分异构体一共有___种,A与B反应生成的另一种含六元环的化合物的结构简式为___。
(3)②反应的类型为___,③反应的化学方程式为:___。
(4)按下列要求写出B的两种同分异构体的结构简式:___。
(Ⅰ)能发生银镜反应;(Ⅱ)分子结构中含有两个甲基;(Ⅲ)能发生水解反应
由丙烯制得B经如下流程:CH3-CH=CH2![]() CH3CHClCH2Cl
CH3CHClCH2Cl![]() C→X→Y→Z→CH2=CH-COOH
C→X→Y→Z→CH2=CH-COOH![]() B
B
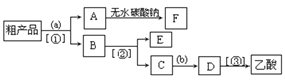
(5)参照流程中的前两步和最后一步的书写方法写出其他中间步骤的流程:_____。
【答案】2-甲基-1,3-丁二烯 CH2=CHCOOCH2CH3 3 ![]() 加成反应
加成反应 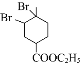 +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O HCOOCH=C(CH3)2、HCOOC(CH3)=CHCH3 CH3CHOHCH2OH
+2NaBr+2H2O HCOOCH=C(CH3)2、HCOOC(CH3)=CHCH3 CH3CHOHCH2OH![]() CH3COCHO
CH3COCHO![]() CH3COCOOH
CH3COCOOH![]() CH3CHOHCOOH
CH3CHOHCOOH![]() CH2=CH-COOH
CH2=CH-COOH
【解析】
A为天然橡胶的单体,分子式为C5H8,则A为2-甲基-1,3-丁二烯,结构简式为:CH2=C(CH3)CH=CH2,A、B发生信息中的反应,则B为CH2=CHCOOCH2CH3,反应②为加成反应,其产物结构简式为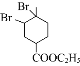 ,然后发生消去反应生成M;
,然后发生消去反应生成M;
(5)丙烯和氯气发生加成反应生成CH3CHClCH2Cl,CH3CHClCH2Cl发生水解反应生成C为CH3CHOHCH2OH,C发生催化氧化生成X为CH3COCHO,X发生催化氧化反应生成Y为CH3COCOOH,Y与H2发生加成反应生成Z为CH3CHOHCOOH,Z发生消去反应生成丙烯酸,丙烯酸和乙醇发生酯化反应生成B。
由上述分析可知A为CH2=C(CH3)CH=CH2,B为CH2=CHCOOCH2CH3,分子式为C10H16Br2O2的物质是 ,M为
,M为![]() 。
。
(1)A为CH2=C(CH3)CH=CH2,A的名称是2-甲基-1,3-丁二烯,B结构简式是CH2=CHCOOCH2CH3;
(2) A为CH2=C(CH3)CH=CH2,A的属于炔烃的同分异构体有三种,碳链结构为C≡C-C-C-C、![]() 、C-C≡C-C-C;A与B反应生成的另一种含六元环的化合物的结构简式为
、C-C≡C-C-C;A与B反应生成的另一种含六元环的化合物的结构简式为![]() ;
;
(3)②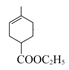 与Br2发生加成反应产生
与Br2发生加成反应产生 ,所以②反应的类型为加成反应;③反应为消去反应,反应的化学方程式为:
,所以②反应的类型为加成反应;③反应为消去反应,反应的化学方程式为: +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O;
+2NaBr+2H2O;
(4)B为CH2=CHCOOCH2CH3,B的同分异构体符合下列条件:
(Ⅰ)能发生银镜反应,说明含有醛基;
(Ⅱ)分子结构中含有两个甲基;
(Ⅲ)能发生水解反应,说明含有酯基,含有HCOO-,
符合条件的结构简式为HCOOCH=C(CH3)2、HCOOC(CH3)=CHCH3;
(5)丙烯和氯气发生加成反应生成CH3CHClCH2Cl,产物发生水解反应生成C为CH3CHOHCH2OH,C发生催化氧化生成X为CH3COCHO,X发生催化氧化反应生成Y为CH3COCOOH,Y与H2发生加成反应生成Z为CH3CHOHCOOH,Z再发生消去反应生成丙烯酸CH2=CH-COOH,丙烯酸和乙醇发生酯化反应生成B,其合成路线为CH3CHOHCH2OH![]() CH3COCHO
CH3COCHO![]() CH3COCOOH
CH3COCOOH![]() CH3CHOHCOOH
CH3CHOHCOOH![]() CH2=CH-COOH。
CH2=CH-COOH。

【题目】某学生为探究锌与盐酸反应过程中的速率变化,在![]() 时,向100 mL 2 mol·L-1盐酸中加入过量的锌粉,测得氢气体积(已换算成标准状况)累计值如下:
时,向100 mL 2 mol·L-1盐酸中加入过量的锌粉,测得氢气体积(已换算成标准状况)累计值如下:
时间(min) | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(1)①在2~3 min时间段内,用盐酸的浓度变化表示的反应速率为_______.
②在0~5min内,反应速率最大的时间段是___(填 “1~2 min”、“2~3 min”或“3~4 min”)。
(2)若完全反应后放出15.2 kJ的热量,则反应Zn(s) + 2HCl(aq)=ZnCl2(aq) + H2(g)的△H=____
(3)为了减缓反应速率但不减少产生气体的量,可向反应物中分别加入等体积的下列液体,你认为可行的是_______(填字母)。
a. 蒸馏水 b. Na2CO3溶液 c. NaNO3溶液
(4)为了加快反应速率但不减少产生气体的量,某同学向反应物中加入了少量CuSO4固体,该同学操作____(填 “合理”或“不合理”),理由是_______