题目内容
(11分)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,且不会造成二次污染。已知高铁酸盐热稳定性差,工业上用湿法制备高铁酸钾的基本流程如下图所示:
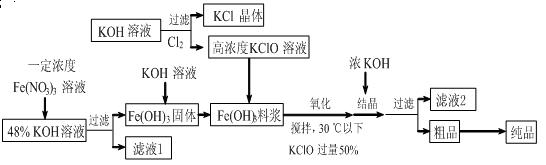
(1)上述氧化过程中,发生反应的离子方程式是: ,控制反应温度30℃以下的原因是: 。
(2)结晶过程中加入浓KOH溶液的作用是: 。
(3)根据图1、图2回答:为了获取更多的高铁酸钾,铁盐的质量分数应控制在 附近、反应时间应控制在 。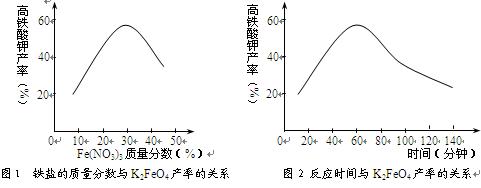

(1)上述氧化过程中,发生反应的离子方程式是: ,控制反应温度30℃以下的原因是: 。
(2)结晶过程中加入浓KOH溶液的作用是: 。
(3)根据图1、图2回答:为了获取更多的高铁酸钾,铁盐的质量分数应控制在 附近、反应时间应控制在 。

(1)2Fe(OH)3+3ClO-+4OH-===2FeO42-+3Cl-+5H2O (3分)
防止生成的K2FeO4发生分解(2分)
(2)增大K+浓度,促进K2FeO4晶体析出 (2分)
(3)30% (2分) 60min(2分)
防止生成的K2FeO4发生分解(2分)
(2)增大K+浓度,促进K2FeO4晶体析出 (2分)
(3)30% (2分) 60min(2分)
略

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

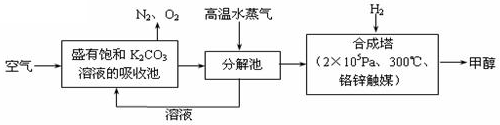
 科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇(分子式为CH3OH)。“绿色自由”构想技术流程如下:
科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇(分子式为CH3OH)。“绿色自由”构想技术流程如下: