题目内容
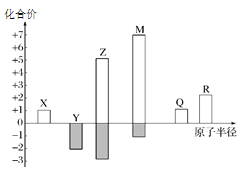
【题目】X、Y、Z、M、Q、R皆为前20号元素,其原子半径与化合价的关系如图所示。下列说法错误的是( )
A.Q位于第三周期ⅠA族
B.X、Y、Z三种元素组成的化合物可能是盐或碱
C.Z与M的最高价氧化物对应水化物均为强酸
D.简单离子半径:M->Q+>R2+
【答案】D
【解析】
X、Y、Z、M、Q、R皆为前20号元素,Y的化合价只有-2价,则Y为O元素;X的原子半径比Y的原子半径小且只有+1价,则X为H元素; M的最高正价为+7价,最低负价为-1价,因为F没有正价,所以M为C1元素;Z元素最低负价为-3价,最高价为+5价,且Z的原子半径小于M的原子半径,则Z为N元素; Q只有+1价,R只有+2价,Q、R的原子半径均大于M的原子半径,且R的原子半径大于Q的原子半径,故Q为Na元素,R为Ca元素,综上, X为H元素, Y为O元素, Z为N元素,M为C1元素,Q为Na.元素,R为Ca元素。
A.由分析可知,Q为Na元素,位于第三周期IA族, A正确;
B.由分析可知,X、Y、Z分别为H、O、N,可以形成HNO3、NH4NO3、NH3H2O,HNO3属于酸、NH4NO3属于盐、NH3H2O属于碱,B正确;
C.由分析可知,Z、M分别为N、Cl,最高价氧化物对应的水化物分别为HNO3和HClO4,都是强酸,C正确;
D.由分析可知,M、Q、R分别为:Cl、Na、Ca,简单离子分别为Cl-、Na+、Ca2+,根据“层多径大、序大径小”,离子半径:M->R2+>Q+, D错误;
故选D。

【题目】现有部分短周期元素的性质或原子结构如表:
元素编号 | 元素性质或原子结构 |
T | M层上有6个电子 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 元素最高正价是+7价 |
W | 其单质既能跟酸反应,又能跟强碱反应,都产生H2 |
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是_____。
(2)元素Y与氢元素形成一种离子YH4+,写出该微粒的电子式_____,如何检验某溶液中含该离子_____。
(3)元素Z在周期表中的位置_____,元素Z与元素T相比,非金属性较强的是_____(用元素符号表示),下列表述中能证明这一事实的是_____(填序号)。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下,Z和T的单质都能与氢氧化钠溶液反应