��Ŀ����
����Ŀ����������֪��3(NH4)2SO4![]() 4NH3��+3SO2��+N2+6H2O��ij�������Ա��ѡ������װ��̽������淋�����(��װ����ҩƷ����)��
4NH3��+3SO2��+N2+6H2O��ij�������Ա��ѡ������װ��̽������淋�����(��װ����ҩƷ����)��
�ش��������⣺
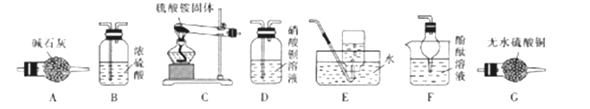
(1)Aװ��ʢװ��ʯ�ҵ�������_________��Cװ���д��Թ�������б��ԭ����__________________��
(2)����ͬѧ��Ʒ�����C��G��B��D��E��
����֤����ˮ���ɵ�ʵ��������_______________��Bװ�õ�������______________��
��ʵ���У��۲쵽Dװ���в�����ɫ������ʵ����Ϻ���Dװ���л����ð�ɫ������Ϊ�˼����ɫ������BaSO4����BaSO3����Ƽ�ʵ�鷽����________________��
��Dװ���з�����Ӧ�����ᱵ�����йأ������ᱵ��������D�з�Ӧ�����ӷ���ʽΪ_______________��
�ܸ�ʵ�鷽����֤������淋ķֽ������______________(�ѧʽ)��
(3)����ͬѧѡ������װ��֤�������Ƿ���NH3��
������������ң�װ������˳��ΪC��__________��
����֤���а������ɵ�ʵ��������________________��
(4)����ͬѧ���ʵ��ⶨ�������Ʒ�Ĵ���(���ʲ��μӷ�Ӧ)��ȡ15.0g��Ʒ��������ˮ�����������Ȼ�����Һ��ϡ���ᣬ���ˡ�ϴ�ӡ�������أ�BaSO4����Ϊ23.3g������Ʒ������淋���������Ϊ________(���������λС��)��
���𰸡� ����� ��Ʒ�ֽ�������ˮ����ֹ�Թ�ը�� Gװ���а�ɫ��ĩ�����ɫ ���հ��� ȡ������ɫ�������Թܣ��μ��������ᣬ����ɫ�����ܽ⣬����BaSO3����֮����BaSO4 3Ba2++2NO3- +3SO2+2H2O=3BaSO4��+2NO+4H+ H2O��SO2��N2 A��F ��ɫ��̪��Һ��� 88%
��������(1). Aװ��ʢװ��ʯ�ҵ������Ǹ���ܡ�Cװ���д��Թ�������б��ԭ������Ʒ�ֽ�������ˮ����ֹ�Թ�ը�ѡ�
(2). ����ͬѧ��Ʒ�����C��G��B��D��E��
����֤����ˮ���ɵ��ǰ�ɫ��ˮ����ͭ��ĩ��ˮ��Ӧ������ɫ�ľ��壬����ʵ��������Gװ���а�ɫ��ĩ�����ɫ��Bװ�õ����������հ�����
��ʵ���У��۲쵽Dװ���в�����ɫ������ʵ����Ϻ���Dװ���л����ð�ɫ������Ϊ�˼����ɫ������BaSO4����BaSO3����Ƽ�ʵ�鷽����ȡ������ɫ�������Թܣ��μ��������ᣬ����ɫ�����ܽ⣬����BaSO3����֮����BaSO4 ��
��Dװ���з�����Ӧ�����ᱵ�����йأ������ᱵ��������D�з�Ӧ�����ӷ���ʽΪ3Ba2++2NO3- +3SO2+2H2O=3BaSO4��+2NO+4H+��
�ܸ�ʵ�鷽����Gװ����֤����ˮ���ɣ�Dװ����֤���ж����������ɣ����Eװ������ˮ���ռ���������֤���е������ɣ����Ը�ʵ�鷽����֤������淋ķֽ������H2O��SO2��N2��
(3). ����ͬѧѡ������װ��֤�������Ƿ���NH3�����Խ����ɵ�������ͨ��Aװ���ü�ʯ�ҰѶ����������պ���ͨ��Fװ�ã����а�������������ˮ��������һˮ�ϰ��Լ���ʹ��̪��졣
������������ң�װ������˳��ΪC��A��F��
����֤���а������ɵ�ʵ����������ɫ��̪��Һ��졣
(4). ����ͬѧ���ʵ��ⶨ�������Ʒ�Ĵ���(���ʲ��μӷ�Ӧ)��ȡ15.0g��Ʒ��������ˮ�����������Ȼ�����Һ��ϡ���ᣬ���ˡ�ϴ�ӡ�������أ�BaSO4����Ϊ23.3g��������ᱵ�����ʵ���Ϊ0.1mol������������غ��������淋����ʵ���Ϊ0.1mol�����������淋�����Ϊ13.2g �������ø���Ʒ������淋���������Ϊ![]() 88%��
88%��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ�������ڰ칫�һ��Ǿ������Ư���Ļ�ƿ�в���һ���������ʻ�����������Ŷ���æµ�Ĺ���������������ɺ����õ����顣����ڻ�ƿ�м��롰�ʻ����ʼ������ͻ��ӳ��ʻ����������±���1L���ʻ����ʼ����ijɷ֣��Ķ���ش��������⣺
�ɷ� | ����(g) | Ħ������(mol��L-1) |
���� | 50.00 | 342 |
����� | 0.50 | 174 |
��˾ƥ�� | 0.35 | 180 |
������� | 0.50 | 158 |
������ | 0.04 | 170 |
��1�����ʻ����ʼ�����K+�����ʵ���Ũ��Ϊ����˾ƥ���в���K+��__________��ֻҪ��д����ʽ��������㣩mol��L-1��
��2�����ƹ����У����в������ƽ��û��Ӱ�����________������ĸ����
A������ƿ��ʹ��ǰδ�����������������ˮ
B������ʱ����Һ��
C������ƿ��ʹ��ǰ�ո�������һ�����ʵ���Ũ�ȵ�NaC1��Һ��δϴ��
D������ҡ�Ⱥ���Һ���������ƿ�Ŀ̶��ߣ���δ���κδ���