��Ŀ����
��0.1000mol/L�ı�����ֱ�ζ�20.00mL��0.1000mol/L��ˮ��20.00mL��0.1000mol/L����������Һ�ĵζ�������ͼ��ʾ��������Ϊ�ζ��ٷ������ζ��������ܵζ���������������Ϊ�ζ���������ҺpH��������һ�����ָʾ������ɫ��ΧΪ4.4-6.2�������йصζ�����˵����ȷ����
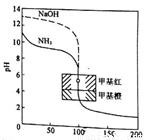
A. �ζ���ˮ��Һ���ζ�����Ϊ50��ʱ��������Ũ�ȼ���ڹ�ϵ��c(NH4+)+c(H+)=c(OH-)
B. �ζ�����Ϊ100��ʱ����Ϊ�ζ������з�Ӧǡ����ȫ��ʱ��
C. �ӵζ����߿����жϣ�ʹ�ü�����Ϊ�ζ������е�ָʾ��ȷ�Ը���
D. �ζ���ˮ��Һ���ζ�����Ϊ150��ʱ��������Һ������Ũ���д�С��ϵc(Cl-)��c(H+)
 Ʒѧ˫�ž�ϵ�д�
Ʒѧ˫�ž�ϵ�д� Сѧ��ĩ���100��ϵ�д�
Сѧ��ĩ���100��ϵ�д� ��ĩ��ϰ���ϵ�д�
��ĩ��ϰ���ϵ�д� ����ѧ�䵥Ԫ������ĩר����100��ϵ�д�
����ѧ�䵥Ԫ������ĩר����100��ϵ�д�ij��ҵ��ˮ�н����±������е�5�֣�
������ | K+ Cu2+ Fe3+ Ca2+ Fe2+ |
������ | Cl- CO32- NO3- SO42- SiO32- |
ijͬѧ��̽����ˮ����ɣ�����������ʵ�飺
��ȡ��ˮ���������������ᣬ�ް�ɫ��������,��������ʹ����ʯ��ˮ����ǵ���ɫ��ζ����
����������õ���Һ�м���BaCl2��Һ���а�ɫ�������ɡ�
�����ƶϲ���ȷ����
A. ��Һ��һ�����е���������K+ �� Cl- ��CO32- ��NO3- �� SO42-
B. ���м�������������ɫ����ĵ����ӷ���ʽ��CO32-+2H+=CO2��+H2O
C. ԭ��Һ�е�K+ �� Cl- ��NO3- ���������ȷ��
D. ���в�����ɫ���������ӷ���ʽ��Ba2++SO42-=BaSO4��


 C6+LiCoO2,�乤��ԭ����ͼ�����й��ڸõ�ص�˵����ȷ����
C6+LiCoO2,�乤��ԭ����ͼ�����й��ڸõ�ص�˵����ȷ����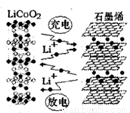


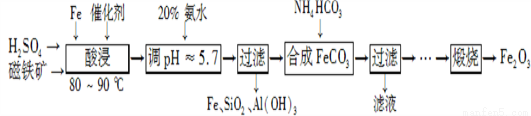
 _______________________________________________��
_______________________________________________�� ���IJ�Ʒ����
���IJ�Ʒ����