题目内容
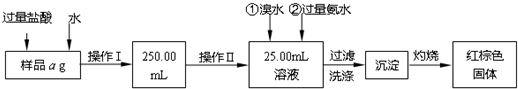
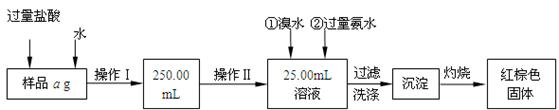
某氯化铁与氯化亚铁的混合物。现要测定其中铁元素的质量分数,实验按以下步骤进行:

Ⅰ.请根据上面流程,回答以下问题:
(1)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有 、 ,(填仪器名称)
(2)请写出加入溴水发生的离子反应方程式 ,
(3)将沉淀物加热,冷却至室温,用天平称量其质量为b1 g,再次加热并冷却至室温称量其质量为b2 g,若b1-b2=0.3g,则接下来还应进行的操作是
。
若蒸发皿质量是W1 g,蒸发皿与加热后固体总质量是W2 g,则样品中铁元素的质量分数是
Ⅱ.有同学提出,还可以采用以下方法来测定:

(1)溶解样品改用了硫酸,而不用盐酸,为什么
(2)选择的还原剂是否能用铁 (填“是”或“否”),原因是:
(3)若滴定用掉c mol/L KMnO4溶液bmL,则样品中铁元素的质量分数是
Ⅰ.(1)250mL容量瓶(1分)、胶头滴管(1分)
(2)2Fe 2+ + Br2 = 2Fe 3+ + 2Br-(2分)
(3)再次加热冷却并称量,直至两次质量差小于0.1g(2分)
铁元素的质量分数是![]() (3分)
(3分)
Ⅱ.(1)过量的盐酸对后面KMnO4的滴定有干扰(1分)
(2)否(1分)如果用铁做还原剂,会与过量的硫酸反应生成Fe2+,干扰铁元素的测定(2分)
(3)铁元素的质量分数是2.8bc/a(2分)
解析:
略