��Ŀ����
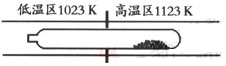
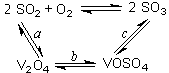
��1����������Ĵ������Ĺ�����ͼ��ʾ������a��c�����Ļ�ѧ����ʽ�ɱ�ʾΪ��
SO2+V2O5 SO3+ V2O4
SO3+ V2O4
4VOSO4+O2 2V2O5+4SO3��
2V2O5+4SO3��
�÷�Ӧ�Ĵ����� ��д��ѧʽ��
��2�� 550 ��ʱ��SO2ת��ΪSO3��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ��ʾ����2��0 mol SO2��1��0 mol O2����5 ���ܱ������У���Ӧ��ƽ�����ϵ��ѹǿΪ0��10 M Pa���Լ��㷴Ӧ2SO3 2SO2+O2��550 ��ʱ��ƽ�ⳣ��K= ��
2SO2+O2��550 ��ʱ��ƽ�ⳣ��K= ��

��3��550 ��ʱ����2��0 mol SO2��1��0 mol O2����5 ���ܱ������У���Ӧ ��ƽ������д�ʩ����ʹn(SO3)/n(SO2)�������
A�������¶�
B������He(g)��ʹ��ϵ��ѹǿ����
C���ٳ���2 mol SO2��1 mol O2
D���ٳ���1 mol SO2��1 mol O2
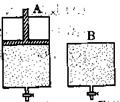
��4��ά���¶Ȳ���������ʹ֮�������·�Ӧ��2SO2��O2 2SO3������ֻ�ܱ�����A��B��A������һ�������ƶ��Ļ�����ʹ�����ڱ��ֺ�ѹ��B�����ܱ��ֺ��ݡ���ʼʱ�������������зֱ��������ʵ����������Ϊ2��1��SO2��O2�Ļ�����壬��ʹA��B�ݻ���ȣ�����ͼ��ʾ����
2SO3������ֻ�ܱ�����A��B��A������һ�������ƶ��Ļ�����ʹ�����ڱ��ֺ�ѹ��B�����ܱ��ֺ��ݡ���ʼʱ�������������зֱ��������ʵ����������Ϊ2��1��SO2��O2�Ļ�����壬��ʹA��B�ݻ���ȣ�����ͼ��ʾ����
����д���пո�
A�����ﵽƽ��ʱ�����ʱ���B����__________������̻�����ƽ��ʱA������SO2��ת���ʱ�B����_______��������С�������ﵽ����ƽ���������������ͨ������ʵ�����ԭ��Ӧ���壬�ﵽƽ��ʱ��A�����Ļ��������SO3���������_________�����������С�����䡱����ͬ����B�����Ļ��������SO3���������_________��

SO2+V2O5
 SO3+ V2O4
SO3+ V2O44VOSO4+O2
 2V2O5+4SO3��
2V2O5+4SO3���÷�Ӧ�Ĵ����� ��д��ѧʽ��
��2�� 550 ��ʱ��SO2ת��ΪSO3��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ��ʾ����2��0 mol SO2��1��0 mol O2����5 ���ܱ������У���Ӧ��ƽ�����ϵ��ѹǿΪ0��10 M Pa���Լ��㷴Ӧ2SO3
 2SO2+O2��550 ��ʱ��ƽ�ⳣ��K= ��
2SO2+O2��550 ��ʱ��ƽ�ⳣ��K= ��
��3��550 ��ʱ����2��0 mol SO2��1��0 mol O2����5 ���ܱ������У���Ӧ ��ƽ������д�ʩ����ʹn(SO3)/n(SO2)�������
A�������¶�
B������He(g)��ʹ��ϵ��ѹǿ����
C���ٳ���2 mol SO2��1 mol O2
D���ٳ���1 mol SO2��1 mol O2
��4��ά���¶Ȳ���������ʹ֮�������·�Ӧ��2SO2��O2
 2SO3������ֻ�ܱ�����A��B��A������һ�������ƶ��Ļ�����ʹ�����ڱ��ֺ�ѹ��B�����ܱ��ֺ��ݡ���ʼʱ�������������зֱ��������ʵ����������Ϊ2��1��SO2��O2�Ļ�����壬��ʹA��B�ݻ���ȣ�����ͼ��ʾ����
2SO3������ֻ�ܱ�����A��B��A������һ�������ƶ��Ļ�����ʹ�����ڱ��ֺ�ѹ��B�����ܱ��ֺ��ݡ���ʼʱ�������������зֱ��������ʵ����������Ϊ2��1��SO2��O2�Ļ�����壬��ʹA��B�ݻ���ȣ�����ͼ��ʾ����
����д���пո�
A�����ﵽƽ��ʱ�����ʱ���B����__________������̻�����ƽ��ʱA������SO2��ת���ʱ�B����_______��������С�������ﵽ����ƽ���������������ͨ������ʵ�����ԭ��Ӧ���壬�ﵽƽ��ʱ��A�����Ļ��������SO3���������_________�����������С�����䡱����ͬ����B�����Ļ��������SO3���������_________��
��1��V2O5����2��400 L?mol-1����3��CD����4���̣����䣻����
�����������1�����������Ϣ��ϴ������뻯ѧ��Ӧ�Ļ�������������ΪV2O5����2�����ݻ�ѧƽ����������ʽ���м��㣬�����ͼ��֪����ϵ��ѹǿΪ0.10M Pa����ʱ���������ת����Ϊ80%�� 2SO2��O2
 2SO3
2SO3��ʼ����mol�� 2 1 0
�仯�� ��mol��2��0.8 0.8 2��0.8
ƽ���� ��mol�� 0.4 0.2 1.6
ƽ��ʱ�����ʵ�Ũ��Ϊ��[SO2]=0.08mol/L��[O2]=0.04mol/L��[SO3]="0.32mol/L" ����ƽ�ⳣ���ı���ʽ����õ�ƽ�ⳣ��K="400" L?mol-1����3��550 ��ʱ����2��0 mol SO2��1��0 mol O2����5 ���ܱ������У���Ӧ��ƽ���Ҫʹn(SO3)/n(SO2)����ƽ�����������ƶ���A���÷�Ӧ����Ϊ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ�������B������He(g)��ʹ��ϵ��ѹǿ�����뷴Ӧ��ص�����Ũ�Ȳ��䣬ƽ�ⲻ�ƶ�������C���ٳ���2 mol SO2��1 mol O2���൱�ڼ�ѹ��ƽ�������ƶ�����ȷ��D���ٳ���1 mol SO2��1 mol O2��ƽ�������ƶ�����ȷ��ѡCD����4����A�������ֺ�ѹ����Ӧ�����������С��Ũ��������Ũ��Խ��ѧ��Ӧ����Խ�죬����ƽ���ʱ��Խ�̣����Դﵽƽ������ʱ��A��B�̣�A����������٣�ѹǿ����ƽ��������Ӧ�����ƶ�������A��SO2��ת���ʱ�B������������ͨ�������ԭ��Ӧ���壬�ﵽƽ���A�н�����ƽ����ԭƽ���Ч������SO3������������䣬B�����н�����ƽ���൱����ԭƽ��Ļ���������ѹǿ��ƽ�������ƶ���B������SO3�������������

��ϰ��ϵ�д�
 ���ݼ���ϵ�д�
���ݼ���ϵ�д�
�����Ŀ
 2CrO42-��2H+����K2Cr2O7����ˮ���ϡ��Һ�dz�ɫ��
2CrO42-��2H+����K2Cr2O7����ˮ���ϡ��Һ�dz�ɫ��


 2C��g��һ��ʱ���ﵽƽ�⣬����n mol C��������˵���в���ȷ���ǣ� ��
2C��g��һ��ʱ���ﵽƽ�⣬����n mol C��������˵���в���ȷ���ǣ� ��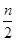 ��
�� 2C(g) ��H=��QkJ/mol���мס��������ݻ���ͬ�Ҳ�����ܱ���������������м���1 mol A��3 mol B����һ�������´ﵽƽ��ʱ�ų�����ΪQ1kJ������ͬ�������£����������м���2 mol C�ﵽƽ�����������ΪQ2 kJ����֪Q1=3Q2��������������ȷ���ǣ� ��
2C(g) ��H=��QkJ/mol���мס��������ݻ���ͬ�Ҳ�����ܱ���������������м���1 mol A��3 mol B����һ�������´ﵽƽ��ʱ�ų�����ΪQ1kJ������ͬ�������£����������м���2 mol C�ﵽƽ�����������ΪQ2 kJ����֪Q1=3Q2��������������ȷ���ǣ� ��


 cC(g)+dD(g)��C�İٷֺ���(C%)���¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ�����и÷�Ӧ�Ħ�H�ͦ�S�ж���ȷ����(����)
cC(g)+dD(g)��C�İٷֺ���(C%)���¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ�����и÷�Ӧ�Ħ�H�ͦ�S�ж���ȷ����(����)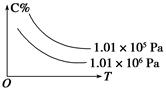
 TaI4 (g)+S2 (g)
TaI4 (g)+S2 (g)