题目内容
(14分)完成下列各题:(1).在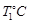 时,向容积为2L的密闭容器甲中加入1molN2、3molH2及少量固体催化剂,发生反应N2(g)+3H2(g)
时,向容积为2L的密闭容器甲中加入1molN2、3molH2及少量固体催化剂,发生反应N2(g)+3H2(g) 2NH3(g);
2NH3(g);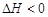 ,10min时各物质的浓度不再变化,测得NH3的物质的量为0.4mol。
,10min时各物质的浓度不再变化,测得NH3的物质的量为0.4mol。
①该反应在0~10min时间内H2的平均反应速率为 N2的转化率为
②在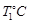 时,若起始时在容器甲中加入0.5molN2、1.5 molH2、1 molNH3,则达到平衡时NH3的物质的量为( )(填选项字母)
时,若起始时在容器甲中加入0.5molN2、1.5 molH2、1 molNH3,则达到平衡时NH3的物质的量为( )(填选项字母)
a 大于0.4mol b 等于0.4mol c 小于0.4mol
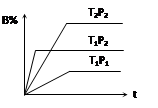
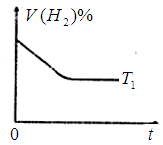
③下图是在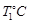 时密闭容器甲中H2的体积分数随时间t的变化曲线,请在该图中补画出该反应在
时密闭容器甲中H2的体积分数随时间t的变化曲线,请在该图中补画出该反应在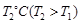 时的H2体积分数随时间t的变化曲线。
时的H2体积分数随时间t的变化曲线。
(2).已知:Al3 +与HCO3–、CO32–、HS-、S2-等能发生彻底的
双水解,生活中通常利用Al3 +与HCO3–的反应来制作泡沫灭火器。泡沫灭火器的简易构造如下图,a为玻璃瓶,b为铁筒,请思考:
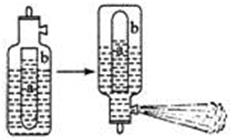
①参与反应的液体分别为Al2(SO4)3和NaHCO3,请问a瓶中盛放的液体为: 。
②为了保证泡沫灭火器的使用寿命,通常在Al2(SO4)3溶液中加入另一种物质抑制硫酸铝的水解,请问该物质是 。
③已知苯酚是比碳酸更弱的酸,请问,苯酚钠和硫酸铝能否发生彻底的双水解?如能,请写出该反应的离子反应方程式: 。
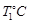 时,向容积为2L的密闭容器甲中加入1molN2、3molH2及少量固体催化剂,发生反应N2(g)+3H2(g)
时,向容积为2L的密闭容器甲中加入1molN2、3molH2及少量固体催化剂,发生反应N2(g)+3H2(g) 2NH3(g);
2NH3(g);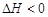 ,10min时各物质的浓度不再变化,测得NH3的物质的量为0.4mol。
,10min时各物质的浓度不再变化,测得NH3的物质的量为0.4mol。①该反应在0~10min时间内H2的平均反应速率为 N2的转化率为
②在
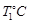 时,若起始时在容器甲中加入0.5molN2、1.5 molH2、1 molNH3,则达到平衡时NH3的物质的量为( )(填选项字母)
时,若起始时在容器甲中加入0.5molN2、1.5 molH2、1 molNH3,则达到平衡时NH3的物质的量为( )(填选项字母)a 大于0.4mol b 等于0.4mol c 小于0.4mol
③下图是在
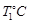 时密闭容器甲中H2的体积分数随时间t的变化曲线,请在该图中补画出该反应在
时密闭容器甲中H2的体积分数随时间t的变化曲线,请在该图中补画出该反应在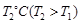 时的H2体积分数随时间t的变化曲线。
时的H2体积分数随时间t的变化曲线。
(2).已知:Al3 +与HCO3–、CO32–、HS-、S2-等能发生彻底的
双水解,生活中通常利用Al3 +与HCO3–的反应来制作泡沫灭火器。泡沫灭火器的简易构造如下图,a为玻璃瓶,b为铁筒,请思考:

①参与反应的液体分别为Al2(SO4)3和NaHCO3,请问a瓶中盛放的液体为: 。
②为了保证泡沫灭火器的使用寿命,通常在Al2(SO4)3溶液中加入另一种物质抑制硫酸铝的水解,请问该物质是 。
③已知苯酚是比碳酸更弱的酸,请问,苯酚钠和硫酸铝能否发生彻底的双水解?如能,请写出该反应的离子反应方程式: 。
(1)① 0.03mol·L-1 ·min-1 20%
② b ③画在图上 (2)①Al2(SO4)3 ②H2SO4
③ 能 Al3++3C6H5O-+3H2O=Al(OH)3+3C6H5OH↓
② b ③画在图上 (2)①Al2(SO4)3 ②H2SO4
③ 能 Al3++3C6H5O-+3H2O=Al(OH)3+3C6H5OH↓
(1)①反应速率通常用单位时间内浓度的变化量来表示,平衡时氨气的物质的量是0.4mol,所以消耗氢气是0.6mol,氮气是0.2mol,因此其反应速率为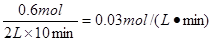 。氮气的转化率为
。氮气的转化率为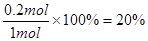 。
。
②根据方程式可知0.5molN2、1.5 molH2、1 molNH3相当于1mol氮气和3mol氢气,因此平衡是等效的,所以氨气的物质的量还是0.4mol。
③因为反应是放热反应,所以升高温度,反应速率增大,到达平衡的水解缩短。但平衡向逆反应方向移动,氢气的含量增大,因此图像为
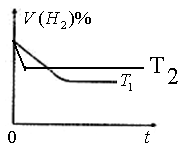
(2)①因为硫酸铝水解显酸性,会腐蚀铁,所以a中放的是硫酸铝,b中放的是碳酸氢钠。
②硫酸铝水解显酸性,因此要抑制其水解,需要加入稀硫酸。
③酸越弱,相应的盐越容易水解,因此苯酚钠和硫酸铝能彻底水解,方程式为Al3++3C6H5O-+3H2O=Al(OH)3+3C6H5OH↓。
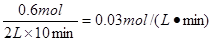 。氮气的转化率为
。氮气的转化率为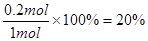 。
。②根据方程式可知0.5molN2、1.5 molH2、1 molNH3相当于1mol氮气和3mol氢气,因此平衡是等效的,所以氨气的物质的量还是0.4mol。
③因为反应是放热反应,所以升高温度,反应速率增大,到达平衡的水解缩短。但平衡向逆反应方向移动,氢气的含量增大,因此图像为

(2)①因为硫酸铝水解显酸性,会腐蚀铁,所以a中放的是硫酸铝,b中放的是碳酸氢钠。
②硫酸铝水解显酸性,因此要抑制其水解,需要加入稀硫酸。
③酸越弱,相应的盐越容易水解,因此苯酚钠和硫酸铝能彻底水解,方程式为Al3++3C6H5O-+3H2O=Al(OH)3+3C6H5OH↓。

练习册系列答案
相关题目
 2NH3(g),下列有关说法不正确的是( )
2NH3(g),下列有关说法不正确的是( ) NaCl(l)+K(g)选取适宜的温度,使K成蒸气从反应混合物中分离出来
NaCl(l)+K(g)选取适宜的温度,使K成蒸气从反应混合物中分离出来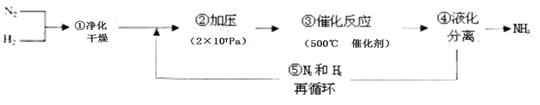
 2NH3,下列有关叙述正确的是
2NH3,下列有关叙述正确的是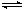 2Z(g) 此反应达到平衡的标志是( )
2Z(g) 此反应达到平衡的标志是( ) PCl3(g)+Cl2 (g)充分反应平衡后,测得PCl5的分解率为a%, 此时,再向密闭容器中加入1mol PCl5 ,充分反应,再次平衡后,下列有关说法正确的是( )
PCl3(g)+Cl2 (g)充分反应平衡后,测得PCl5的分解率为a%, 此时,再向密闭容器中加入1mol PCl5 ,充分反应,再次平衡后,下列有关说法正确的是( )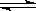 C(g)+3D(g),现从两条途径分别建立平衡,途径Ⅰ:A、B的起始浓度均为2 mol·L—1途径Ⅱ: C、D的起始浓度分别为2 mol·L—1 和6 mol·L—1 ,以下叙述正确的是 ( )
C(g)+3D(g),现从两条途径分别建立平衡,途径Ⅰ:A、B的起始浓度均为2 mol·L—1途径Ⅱ: C、D的起始浓度分别为2 mol·L—1 和6 mol·L—1 ,以下叙述正确的是 ( ) pC(g),在密闭容器中进行,下图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是( )
pC(g),在密闭容器中进行,下图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是( )