��Ŀ����
������ѧ��Ӧ����ʽA+B��X+Y+H2O����ش�
��1����AΪ��ɫ�������ʣ�B��Ũ���ᣬд���÷�Ӧ�Ļ�ѧ����ʽ______����������������X�ķ�����______��
��2����AΪ��ɫ���壬Y�ǻ���ɫ���壬д��Y �ĵ���ʽ______���÷�Ӧ�����ӷ���ʽ��______��������Yͨ��NaOH��Һ�м��ȷ�����Ӧ��������6.72L����״����������ʱ��ת��0.5mol���ӣ�д���÷�Ӧ�Ļ�ѧ����ʽ______��
��3����AΪ�������ʣ�B��ϡ���ᣬ��A��B�����ʵ���֮��Ϊ1��4���з�Ӧ��������ɫ����X��������������Ϊ����ɫ����A������Y��Һ�У�
��д���÷�Ӧ�Ļ�ѧ����ʽ______��
�ں�amolY����Һ�ܽ���һ����A������Һ�����ֽ��������ӵ����ʵ���ǡ����ȣ���ԭ��Y��______mol��
�⣺��1����AΪ��ɫ�������ʣ�ӦΪCu��B��Ũ���ᣬ�����ڼ��������·���������ԭ��Ӧ��������ͭ�Ͷ����������壬��Ӧ�ķ���ʽΪ2H2SO4��Ũ��+Cu  CuSO4+
CuSO4+
2H2O+SO2����SO2����Ư���ԣ���ʹƷ����ɫ���ɽ���ɫSO2ͨ��Ʒ����Һ������ɫ����֤����SO2��
�ʴ�Ϊ��2H2SO4��Ũ��+Cu CuSO4+2H2O+SO2��������ɫSO2ͨ��Ʒ����Һ������ɫ����֤����SO2��
CuSO4+2H2O+SO2��������ɫSO2ͨ��Ʒ����Һ������ɫ����֤����SO2��
��2����AΪ��ɫ���壬Y�ǻ���ɫ���壬ӦΪ�������̺�Ũ����ķ�Ӧ�����ɻ���ɫ����Ϊ����������ʽΪ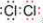 ����Ӧ�����ӷ���ʽΪMnO2+4H++2Cl-
����Ӧ�����ӷ���ʽΪMnO2+4H++2Cl- Mn2++
Mn2++
Cl2��+2H2O��������Cl2ͨ��NaOH��Һ�м��ȷ�����Ӧ��������6.72L����״�������� =0.3mol������ʱ��ת��0.5mol���ӣ�������Ӧ�Ļ�ѧ����ʽΪ
=0.3mol������ʱ��ת��0.5mol���ӣ�������Ӧ�Ļ�ѧ����ʽΪ
6NaOH+3Cl2 NaClO3+5NaCl+3H2O��
NaClO3+5NaCl+3H2O��
�ʴ�Ϊ��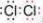 ��MnO2+4H++2Cl-
��MnO2+4H++2Cl- Mn2++Cl2��+2H2O��6NaOH+3Cl2
Mn2++Cl2��+2H2O��6NaOH+3Cl2 NaClO3+5NaCl+3H2O��
NaClO3+5NaCl+3H2O��
��3����AΪ�������ʣ�B��ϡ���ᣬ��A��B�����ʵ���֮��Ϊ1��4���з�Ӧ��������ɫ����X��������������Ϊ����ɫ����A������Y��Һ�У�XΪNO��ͬʱ˵������Ϊ��۽�����ӦΪFe��������Ӧ�Ļ�ѧ����ʽΪFe+4HNO3=NO��+Fe��NO3��3+2H2O����amolFe��NO3��3����Һ�ܽ���һ����Fe������Һ�����ֽ��������ӵ����ʵ���ǡ����ȣ�������ӦΪ2Fe3++Fe=3Fe2+������μӷ�Ӧ��FeΪxmol����μӷ�Ӧ��Fe3+Ϊ2xmol������3x=a-2x��x=0.2a��
�ʴ�Ϊ��Fe+4HNO3=NO��+Fe��NO3��3+2H2O��0.2a��
��������1����AΪ��ɫ�������ʣ�ӦΪCu��B��Ũ���ᣬ�����ڼ��������·���������ԭ��Ӧ��������ͭ�Ͷ����������壻
��2����AΪ��ɫ���壬Y�ǻ���ɫ���壬ӦΪ�������̺�Ũ����ķ�Ӧ�����ɻ���ɫ����Ϊ������
��3����AΪ�������ʣ�B��ϡ���ᣬ��A��B�����ʵ���֮��Ϊ1��4���з�Ӧ��������ɫ����X��������������Ϊ����ɫ����A������Y��Һ�У�XΪNO��ͬʱ˵������Ϊ��۽�����ӦΪFe��
���������⿼��������ƶϣ���Ŀ�Ѷ��еȣ�ע��������ʵ���ɫ��״̬���ص�����жϣ�ѧϰ��ע�����������ʵ����ʣ�
 CuSO4+
CuSO4+2H2O+SO2����SO2����Ư���ԣ���ʹƷ����ɫ���ɽ���ɫSO2ͨ��Ʒ����Һ������ɫ����֤����SO2��
�ʴ�Ϊ��2H2SO4��Ũ��+Cu
 CuSO4+2H2O+SO2��������ɫSO2ͨ��Ʒ����Һ������ɫ����֤����SO2��
CuSO4+2H2O+SO2��������ɫSO2ͨ��Ʒ����Һ������ɫ����֤����SO2����2����AΪ��ɫ���壬Y�ǻ���ɫ���壬ӦΪ�������̺�Ũ����ķ�Ӧ�����ɻ���ɫ����Ϊ����������ʽΪ
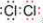 ����Ӧ�����ӷ���ʽΪMnO2+4H++2Cl-
����Ӧ�����ӷ���ʽΪMnO2+4H++2Cl- Mn2++
Mn2++Cl2��+2H2O��������Cl2ͨ��NaOH��Һ�м��ȷ�����Ӧ��������6.72L����״��������
 =0.3mol������ʱ��ת��0.5mol���ӣ�������Ӧ�Ļ�ѧ����ʽΪ
=0.3mol������ʱ��ת��0.5mol���ӣ�������Ӧ�Ļ�ѧ����ʽΪ6NaOH+3Cl2
 NaClO3+5NaCl+3H2O��
NaClO3+5NaCl+3H2O���ʴ�Ϊ��
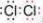 ��MnO2+4H++2Cl-
��MnO2+4H++2Cl- Mn2++Cl2��+2H2O��6NaOH+3Cl2
Mn2++Cl2��+2H2O��6NaOH+3Cl2 NaClO3+5NaCl+3H2O��
NaClO3+5NaCl+3H2O����3����AΪ�������ʣ�B��ϡ���ᣬ��A��B�����ʵ���֮��Ϊ1��4���з�Ӧ��������ɫ����X��������������Ϊ����ɫ����A������Y��Һ�У�XΪNO��ͬʱ˵������Ϊ��۽�����ӦΪFe��������Ӧ�Ļ�ѧ����ʽΪFe+4HNO3=NO��+Fe��NO3��3+2H2O����amolFe��NO3��3����Һ�ܽ���һ����Fe������Һ�����ֽ��������ӵ����ʵ���ǡ����ȣ�������ӦΪ2Fe3++Fe=3Fe2+������μӷ�Ӧ��FeΪxmol����μӷ�Ӧ��Fe3+Ϊ2xmol������3x=a-2x��x=0.2a��
�ʴ�Ϊ��Fe+4HNO3=NO��+Fe��NO3��3+2H2O��0.2a��
��������1����AΪ��ɫ�������ʣ�ӦΪCu��B��Ũ���ᣬ�����ڼ��������·���������ԭ��Ӧ��������ͭ�Ͷ����������壻
��2����AΪ��ɫ���壬Y�ǻ���ɫ���壬ӦΪ�������̺�Ũ����ķ�Ӧ�����ɻ���ɫ����Ϊ������
��3����AΪ�������ʣ�B��ϡ���ᣬ��A��B�����ʵ���֮��Ϊ1��4���з�Ӧ��������ɫ����X��������������Ϊ����ɫ����A������Y��Һ�У�XΪNO��ͬʱ˵������Ϊ��۽�����ӦΪFe��
���������⿼��������ƶϣ���Ŀ�Ѷ��еȣ�ע��������ʵ���ɫ��״̬���ص�����жϣ�ѧϰ��ע�����������ʵ����ʣ�

��ϰ��ϵ�д�
�����Ŀ
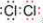
 X+Y+H2O����ش�
X+Y+H2O����ش�