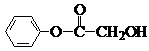题目内容
在CH3COONa溶液中各离子的浓度由大到小排列顺序正确的是( )
| A.c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| B.c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| C.c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D.c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
CH3COONa为强碱弱酸盐,溶液呈碱性,则c(OH-)>c(H+),溶液存在电荷守恒,则c(CH3COO-)+c(OH-)=c(H+)+c(Na+),因此c(Na+)>c(CH3COO-),
因单水解的程度一般较弱,则有c(CH3COO-)>c(OH-),因此有c(Na+)>c(CH3COO-)>c(OH-)>c(H+),
故选A.
因单水解的程度一般较弱,则有c(CH3COO-)>c(OH-),因此有c(Na+)>c(CH3COO-)>c(OH-)>c(H+),
故选A.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
下列说法正确的是( )
| A、100℃时,KW=10-12,此温度下PH=6的溶液一定显酸性 | B、25℃时,0.1mol/L的NaHSO3溶液pH=4,说明HSO3-在水溶液中只存在电离 | C、NH4Cl、CH3COONa、NaHCO3、NaHSO4溶于水,对水的电离都有促进作用 | D、25℃时,10mL 0.1mol/L CH3COOH溶液与5mL 0.1mol/L NaOH溶液混合,所得溶液中有2c(Na+)═c(CH3COO-)+c(CH3COOH) |