��Ŀ����
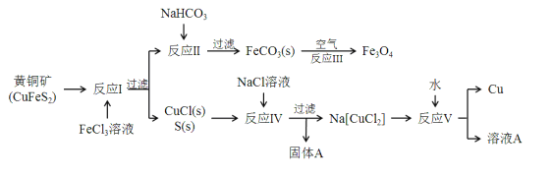
����Ŀ���о����̽����㺬�е�Ag���������������Բ��ƣ�����������е�Ag2O�ȷϾ���Դ�Ļ������������ش���ͼΪ�ӹ�������ȡAg�Ĺ�ҵ���̡���ش��������⡣

��1��NaClO��Һ�����Ȼ������������ֽ⣬��������������80�������½��У����˵ļ��ȷ�ʽΪ________��
��2��NaClO��Һ��Ag��Ӧ�IJ���ΪAgCl��NaOH��O2���÷�Ӧ�Ļ�ѧ����ʽΪ________�����������HNO3����NaClO����Ag���ӷ�Ӧ����ĽǶȷ�������ȱ����________��
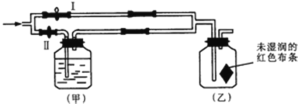
��3�������������Ϊ____���������á�������װ��ϴ���������ʵ�����________��
��4����ѧ�ϳ���10���İ�ˮ�ܽ�AgCl���壬AgCl��NH3��H2O��1�U2��Ӧ������Cl����һ��������________����Һ���������ӵĻ�ѧʽ����ʵ�ʷ�Ӧ�У���ʹ��ˮ����Ҳ���ܽ�AgCl����ȫ���ܽ⣬���ܵ�ԭ����________��
��5������ʱN2H4��H2O��ˮ���£��ڼ����������ܻ�ԭ��4�������ɵ������ӣ�����ת��Ϊ������N2������������0.1 mol��ˮ���¿���ȡ��________g�ĵ���Ag��
��6���Ͼɵ����Ag2O�ܽ��ж������ȩ��HCHO��������CO2����ѧ�Ҿݴ�ԭ���������������Ϊԭ��ػ��յ缫����Ag����Чȥ��������ȩ����˵�ص�������ӦʽΪ________�������IJ�����________��
���𰸡�ˮԡ���� 4Ag+ 4NaClO + 2H2O = 4AgCl + 4NaOH + O2�� ���ɵ��������Ⱦ���� ���� ������������ڹ������ڼ�ˮ��û��ʹˮ��Ȼ���£��ظ�2��3�μ��� [Ag(NH3)2]+ �˷�ӦΪ���淴Ӧ�����ܽ��е��� 43.2 Ag2O + 2e�� + 2H+ = 2Ag + H2O CO2��H+
��������
����ʵ�����̷���ÿ�������Ļ�ѧ��Ӧ����������ÿ��������ԭ�������ݿ��淴Ӧԭ��������𣻸���ԭ���ԭ��������д�缫��Ӧ��
��1����Ҫ���Ʒ�Ӧ�¶����¶���80�����˵ļ��ȷ�ʽΪˮԡ���ȣ��ʴ�Ϊ��ˮԡ���ȣ�
��2�����ݲ�������ˮ�μ��˷�Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪ4Ag+ 4NaClO + 2H2O = 4AgCl + 4NaOH + O2����HNO3��������������ԭ��Ӧ�������л��е������������ɣ���ȱ�������ɵ��������Ⱦ������
�ʴ�Ϊ��4Ag+ 4NaClO + 2H2O = 4AgCl + 4NaOH + O2�������ɵ��������Ⱦ������
��3��������ͼ�п��Կ�������Һ�з�������壬������������Ϊ���ˣ�ϴ�ӵIJ���������Ϊ������������ڹ������ڼ�ˮ��û��ʹˮ��Ȼ���£��ظ�2��3�μ��ɣ�
�ʴ�Ϊ�����ˣ�������������ڹ������ڼ�ˮ��û��ʹˮ��Ȼ���£��ظ�2��3�μ��ɣ���4�������ӺͰ������ӿ����γ��������[Ag(NH3)2]+ ��������ɷ�������ʹ��ˮ����Ҳ������ȫ�ܽ⣬˵���÷�ӦΪ���淴Ӧ��
�ʴ�Ϊ��[Ag(NH3)2]+ ���˷�ӦΪ���淴Ӧ�����ܽ��е��ף�
��5�����е�Ԫ�صĻ��ϼ�Ϊ-2�����������ɵ��������ϼ�Ϊ0������ݵ�ʧ�����غ�ã�n(Ag)=n(N2H4)��2��2=0.1mol��2��2=0.4mol����m(Ag)=108g/mol��0.4mol=43.2g��
�ʴ�Ϊ��43.2g��
��6��ԭ����У������õ��ӣ�������ԭ��Ӧ���缫��ӦΪ��Ag2O + 2e�� + 2H+ = 2Ag + H2O������ʧ���ӣ�����������Ӧ����������Ϊ��CO2��H+��
�ʴ�Ϊ��Ag2O + 2e�� + 2H+ = 2Ag + H2O��CO2��H+��

 �¿α�����Ķ�ѵ��ϵ�д�
�¿α�����Ķ�ѵ��ϵ�д� ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д�