题目内容
10.六六六即六氯环己烷(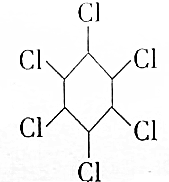 ),是环己烷每个碳原子上的一个氢原子被氯原子取代形成的化合物,下列说法正确的是( )
),是环己烷每个碳原子上的一个氢原子被氯原子取代形成的化合物,下列说法正确的是( )| A. | 六氯环己烷分子中的C原子都是采取sp3杂化 | |
| B. | 六氯环己烷分子中所有C原子共平面 | |
| C. | 六氯环己烷分子中所有原子共平面 | |
| D. | 六氯环己烷不存在同分异构体 |
分析 A.根据价层电子对互斥理论确定中心原子杂化类型,价层电子对个数=σ键个数+孤电子对个数,σ键个数=配原子个数,孤电子对个数=$\frac{1}{2}$(a-xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数.根据n值判断杂化类型:一般有如下规律:当n=2,sp杂化;n=3,sp2杂化;n=4,sp3杂化;
B.环己烷的“稳定结构”是船式和椅式;
C.C原子采取sp3杂化;
D.多个氯原子可以在同一个碳上也可以在不同的碳上.
解答 解:A.中心原子碳原子价层电子对个数=σ键个数+孤电子对个数=4+$\frac{1}{2}$(4-4×1)=4,采取sp3杂化,故A正确;
B.环己烷的“稳定结构”是船式和椅式,所有C原子不共平面,故B错误;
C.C原子采取sp3杂化,为四面体结构,相连的四个原子不在同一平面上,故C错误;
D.多个氯原子可以在同一个碳上也可以在不同的碳上,六氯环己烷存在同分异构体,故D错误.
故选A.
点评 本题考查常见有机化合物的结构以及原子杂化方式的判断,根据价层电子对互斥理论来分析解答即可,题目难度中等.

练习册系列答案
相关题目
1.由NaCl和CuSO4组成的混合溶液中,c(Cl-)=3c(Cu2+)=1.2mol/L,取该混合液100mL,用石墨作电极进行点解,通电一段时间后,在阴极收集到11.2mL(标准状况)的气体.若溶液的体积仍为100mL,此时溶液的pH值为( )
| A. | 1 | B. | 2 | C. | 12 | D. | 13 |
18.下列试剂不能用于除去H2中混有的CO2杂质的是( )
| A. | NaOH溶液 | B. | Na2CO3溶液 | C. | Ba(OH)2溶液 | D. | H2SO4溶液 |
5.关于1mol•L-1 硫酸溶液,下列不正确的是( )
| A. | 1L该溶液中含溶质98g | |
| B. | 从10mL该溶液中取出5mL后,剩余溶液的浓度为1mol•L-1 | |
| C. | 将4.9g浓硫酸加入盛有50mL蒸馏水的烧杯中,充分溶解后就可配得该浓度的硫酸 | |
| D. | 该浓度的硫酸具有酸的通性,可与锌反应制取氢气 |
2.下列各组溶液,不用其他试剂就可以将它们区别开的是( )
| A. | HCl、K2CO3、KOH、K2SO4 | B. | NaNO3、HCl、NH4Cl、KOH | ||
| C. | BaCl2、CaCl2、Na2SO4、KNO3 | D. | K2CO3、KOH、MgSO4、KHSO4 |
19.下列各组中的元素,同属于第3周期的是( )
| A. | 氧、碳、氮 | B. | 钠、铝、硅 | C. | 镁、铝、氧 | D. | 氯、溴、碘 |
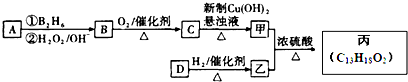
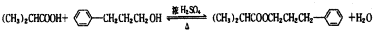 .
. .
.