题目内容
【题目】实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4++6HCHO=3H++6H2O+(CH2)6N4H+[滴定时,1mol(CH2)6N4H+与1molH+相当],然后用NaOH标准溶液滴定反应生成的酸。某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ 称取样品1.500g。
步骤Ⅱ 将样品溶解后,完全转移到250mL容量瓶中,定容,充分摇匀。
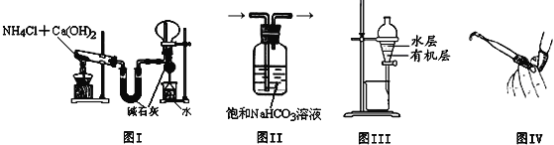
步骤Ⅲ 移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数___(填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积___(填“偏大”、“偏小”或“无影响”)。
对滴定结果的分析最终都是由___的变化来分析C测变化。
③滴定时边滴边摇动锥形瓶,眼睛应观察___。
④滴定达到终点现象__ 。
(2)滴定结果如下表所示:
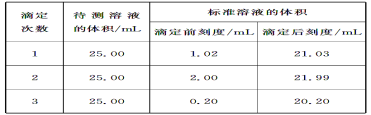
若NaOH标准溶液的浓度为0.1010mol/L,则该样品中氮的质量分数为___。(保留4位有效数字)
【答案】偏高 无影响 溶质物质的量和溶液体积 锥形瓶中溶液颜色变化 当滴入最后一滴标准液,溶液由无色变为浅红色,且半分钟不恢复原来的颜色 18.85%
【解析】
根据题中甲醛法测定(NH4)2SO4样品中氮的质量分数可知,本题考查酸碱滴定,运用酸碱滴定步骤、误差分析方法分析。
(1)①滴定管中未用标准液润洗,直接加入标准液会稀释溶液浓度减小,消耗标准液体积增大,氢离子物质的量增大,4NH++6HCHO=4H++(CH2)6N4+6H2O,反应可知测定氮元素含量偏高,
故答案为:偏高;
②锥形瓶内水对滴定结果无影响,对滴定结果的分析最终都是由溶质物质的量和溶液体积的变化来分析C测变化。
故答案为:无影响;溶质物质的量和溶液体积;
③滴定时边滴边摇动锥形瓶,眼睛应观察锥形瓶中溶液的颜色变化,
故答案为:锥形瓶中溶液颜色变化;
④氢氧化钠滴定酸溶液,达到终点时,当滴入最后一滴标准液,溶液由无色变为浅红色,且半分钟不恢复原来的颜色,
故答案为:当滴入最后一滴标准液,溶液由无色变为浅红色,且半分钟不恢复原来的颜色;
(2)样品1.500g,反应为4NH++6HCHO=4H++(CH2)6N4+6H2O消耗氢离子的物质的量和氮元素物质的量相同,依据图表数据分析可知,三次实验中消耗氢氧化钠溶液体积分别为:20.01mL、19.99mL、20.00mL,三次均有效,氢氧化钠溶液的平均体积为20.00mL;由酸碱中和反应可知,氢离子物质的量=氢氧化钠物质的量=0.1010mol/L×20.00mL×10-3L/mL =2.020×10-3mol,250mL溶液中氮元素物质的量和氢离子物质的量相同,该样品中氮的质量分数=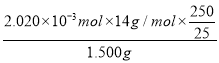 ×100%=18.85%;
×100%=18.85%;
故答案为:18.85%。

【题目】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
Ⅰ.脱硝:
已知H2的燃烧热为285.8kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+133kJ·mol-1
H2O(g)=H2O(l) ΔH=-44kJ·mol-1
催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为___。
Ⅱ.脱碳:(1)向2L密闭容器中加入2molCO2和6molH2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)![]() CH3OH(l)+H2O(l) ΔH<0
CH3OH(l)+H2O(l) ΔH<0
①该反应自发进行的条件是___(填“低温”“高温”或“任意温度”)
②下列叙述能说明此反应达到平衡状态的是___(填字母)。
a.混合气体的平均相对分子质量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1molCO2生成的同时有3 molH—H键断裂
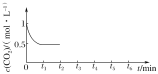
③CO2的浓度随时间(0~t2)变化如图所示,在t2时将容器容积缩小一倍,t3时达到平衡,
t4时降低温度,t5时达到平衡,请画出t2~t6时间段CO2浓度随时间的变化___。
(2)改变温度,使反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH<0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
CH3OH(g)+H2O(g) ΔH<0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
反应Ⅰ: 恒温恒容 | 0min | 2 | 6 | 0 | 0 |
10min | 4.5 | ||||
20min | 1 | ||||
30min | 1 | ||||
反应Ⅱ: 绝热恒容 | 0min | 0 | 0 | 2 | 2 |
①达到平衡时,反应Ⅰ、Ⅱ对比:平衡时CH3OH的浓度c(Ⅰ)___c(Ⅱ)(填“>”“<”或“=”)。
②对反应Ⅰ,前10min内的平均反应速率v(CH3OH)=___。在其他条件不变的情况下,若30 min时只改变温度至T2℃,此时H2的物质的量为3.2mol,则T1___(填“>”“<”或“=”)T2。若30min时只向容器中再充入1 molCO2(g)和1molH2O(g),则平衡___(填“正向”“逆向”或“不”)移动。
(3)利用人工光合作用可将CO2转化为甲酸,反应原理为2CO2+2H2O=2HCOOH+O2,装置如图所示:
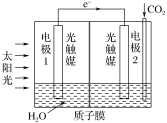
①电极2的电极反应式是____;
②在标准状况下,当电极2室有11.2LCO2反应。理论上电极1室液体质量___(填“增加”或“减少”)___g。