题目内容
下列实验中,操作和现象均正确且能实现相应实验目的的是
选项 | 实验目的 | 操作 | 现象 |
A | 验证BaSO3难溶于水 | 将SO2通人Ba(NO3)2溶液中 | 有白色沉淀生成 |
B | 验证非金属性:Br>I | 将溴水滴加到淀粉KI溶液中 | 溶液变蓝 |
C | 验证SO2的漂白性 | 将SO2通入酸性KMnO4溶液中 | KMnO4溶液褪色 |
D | 验证某化合物一定是钠盐 | 将该化合物在酒精灯上灼烧 | 焰色为黄色 |
A. A B. B C. C D. D
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | Fe3+有氧化性 | 用KSCN溶液可以鉴别Fe3+ |
B | 浓硫酸有腐蚀性 | 常温下浓硫酸不能用铁罐盛装 |
C | Cl2是非金属单质 | Cl2能使湿润的有色布条褪色 |
D | 熔融状态的Al2O3中有自由移动的Al3+和O2- | 电解熔融状态的Al2O3制备Al |
A. A B. B C. C D. D
在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)  2Z(g) △H< 0,一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H< 0,一段时间后达到平衡,反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A. 该温度下此反应的平衡常数K =1.44
B. 其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正)
C. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
D. 0~2min的平均速率ν(Z) = 2.0×10-3mol·L-1·min-1
某温度下,密闭容器中X、Y、Z、W四种气体的初始浓度和平衡浓度如表,下列说法错误的是( )
物质 | X | Y | Z | W |
初始浓度/mol•L﹣1 | 0.5 | 0.6 | 0 | 0 |
平衡浓度/mol•L﹣1 | 0.1 | 0.1 | 0.4 | 0.6 |
A. 反应达到平衡时,X的转化率为80%
B. 该反应的平衡常数表达式为k=
C. 增大压强其平衡常数不变,但使平衡向生成Z的方向移动
D. 改变温度可以改变此反应的平衡常数
在某温度T℃时,将N2O4、NO2分别充入两个各为1L的密闭容器中,反应过程中浓度变化如下[2NO2(g) N2O4(g) △H<0]:
N2O4(g) △H<0]:
容器 | 物质 | 起始浓度/(mol | 平衡浓度/(mol |
Ⅰ | N2O4 | 0.100 | 0.040 |
NO2 | 0 | 0.120 | |
Ⅱ | N2O4 | 0 | 0.0142 |
NO2 | 0.100 | 0.0716 |
下列说法不正确的是( )
A. 平衡时,Ⅰ、Ⅱ中反应的转化率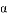 (N2O4)>(NO2)
(N2O4)>(NO2)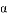
B. 平衡后,升高相同温度,以N2O4表示的反应速率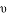 (Ⅰ)<
(Ⅰ)<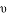 (Ⅱ)
(Ⅱ)
C. 平衡时,Ⅰ、Ⅱ中正反应的平衡常数K(Ⅰ)=
D. 平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深



 ×100%);NaHTeO3溶液的pH__________7(填“ >”、“<”或“=”)。
×100%);NaHTeO3溶液的pH__________7(填“ >”、“<”或“=”)。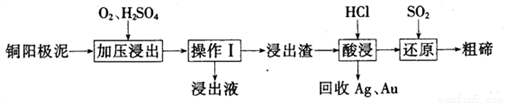
 L-1)
L-1) ,流程图如下:
,流程图如下:

 含有六元环且核磁共振氢谱有4组峰的同分异构体的结构简式________。
含有六元环且核磁共振氢谱有4组峰的同分异构体的结构简式________。