题目内容
【题目】科研人员提出CeO2催化合成DMC需经历三步反应,示意图如图:
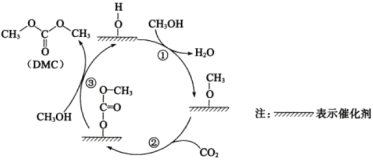
下列说法正确的是( )
A.DMC与过量NaOH溶液反应生成CO32-和甲醇
B.CeO2可有效提高反应物的平衡转化率
C.①、②、③中均有O—H的断裂
D.生成DMC总反应的原子利用率为100%
【答案】A
【解析】
A.DMC为CH3OCOOCH3,属于酯类,酯在碱性条件下可发生水解:CH3OCOOCH3+2NaOH=2CH3OH+Na2CO3,A正确;
B.CeO2为催化剂,催化剂只影响化学反应速率,不影响平衡;所以催化剂不能提高反应物的平衡转化率,B错误;
C.①中CH3OH生成CH3O-催化剂,CH3OH中的O-H键断裂;②中没有O-H键断裂;③CH3OH生成CH3OCOOCH3,CH3OH中的O-H键断裂,C错误;
D.总反应为:2CH3OH+CO2→CH3OCOOCH3+H2O,除了生成DMC外,还生成了水,因此原子利用率不是100%,D错误;
故合理选项是A。

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
【题目】一定条件下,可逆反应2AB+3C,在下列四种状态中,处于平衡状态的是( )
选项 | 正反应速率 | 逆反应速率 |
A | vA=2 mol·L-1·min-1 | vB=2 mol·L-1·min-1 |
B | vA=2 mol·L-1·min-1 | vC=2 mol·L-1·min-1 |
C | vA=1 mol·L-1·min-1 | vB=2 mol·L-1·min-1 |
D | vA=1 mol·L-1·min-1 | vC=1.5 mol·L-1·min-1 |
A. AB. BC. CD. D