题目内容
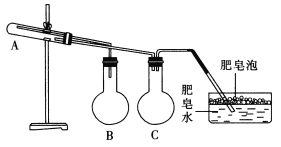
【题目】已知有以下物质的相互转化:

试回答:
(1)B的化学式为_____;D的化学式为_____。
(2)写出由E转变成F的化学方程式:______。
(3)常用____(填试剂名称)检验G中的阳离子,其现象为______。
(4)向G溶液中加入A的有关反应的离子方程式为________。
【答案】FeCl2 KCl 4Fe(OH)2+2H2O+O2=4Fe(OH)3 KSCN溶液 棕黄色溶液变为红色溶液 2Fe3++Fe=3Fe2+
【解析】
白色沉淀在空气中变为红褐色沉淀,可确定白色沉淀E为氢氧化亚铁,红褐色沉淀F为氢氧化铁,G为氯化铁;A与盐酸和G溶液均能生产B溶液,则A为铁,B为氯化亚铁;溶液焰色反应呈紫色,则溶液中含有K元素,则D为氯化钾,C为氢氧化钾;
(1)分析可知,B、D分别为氯化亚铁、氯化钾,其化学式分别为:FeCl2;KCl;
(2)氢氧化亚铁变为氢氧化铁的方程式为:4Fe(OH)2+2H2O+O2=4Fe(OH)3;
(3)常用硫氰化钾检验铁离子的存在,硫氰根离子遇到铁离子溶液显血红色;
(4)铁离子与铁反应生成亚铁离子,离子方程式为2Fe3++Fe=3Fe2+;

 阅读快车系列答案
阅读快车系列答案【题目】低碳经济成为人们一种新的生活理念,二氧化碳的捕捉和利用是能源领域的一个重要研究方向。请你结合下列有关图示和所学知识回答:
(1)用CO2催化加氢可以制取乙烯:CO2(g)+3H2(g)![]() C2H4(g)+2H2O(g)。若该反应体系的能量随反应过程变化关系如图所示,则该反应的ΔH=___(用含a、b的式子表示)。又知:相关化学键的键能如下表所示,实验测得上述反应的ΔH=-152kJ·mol-1,则表中的x=___。
C2H4(g)+2H2O(g)。若该反应体系的能量随反应过程变化关系如图所示,则该反应的ΔH=___(用含a、b的式子表示)。又知:相关化学键的键能如下表所示,实验测得上述反应的ΔH=-152kJ·mol-1,则表中的x=___。

化学键 | C=O | H—H | C=C | C—H | H—O |
键能/kJ·mol-1 | 803 | 436 | x | 414 | 464 |
(2)键能是将1mol理想气体分子AB拆开为中性气态原子A和B所需的能量。已知下列化学键的键能如下表:
化学键 | N≡N | O | N—N | N—H | O—H |
946 | 497 | 193 | 391 | 463 |
写出1mol气态肼(H2N—NH2)燃烧生成氮气和水蒸气的热化学方程式:___。
(3)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。
①科学家提出由CO2制取C的太阳能工艺如图所示。
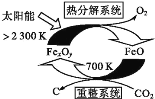
若“重整系统”发生的反应中![]() =6,则FexOy的化学式为___。“热分解系统”中每分解1molFexOy,转移电子的物质的量为___。
=6,则FexOy的化学式为___。“热分解系统”中每分解1molFexOy,转移电子的物质的量为___。
②工业上用CO2和H2反应合成二甲醚。已知:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1,CH3OCH3(g)+H2O(g)=2CH3OH(g) ΔH2=+23.4kJ·mol-1,则2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) ΔH3=___kJ·mol-1。
CH3OCH3(g)+3H2O(g) ΔH3=___kJ·mol-1。