题目内容
3.用排水法收集12ml NO于试管中,然后向倒立于水槽中的该试管内间歇地通入O2共12ml,下面的说法中,正确的是( )| A. | 剩余NO | |
| B. | 剩余NO2 | |
| C. | 试管中气体为红棕色 | |
| D. | 试管内气体先变为红棕色,后红棕色消失,反复几次,最后剩余无色气体. |
分析 根据NO、O2和水反应生成硝酸可知,剩余气体存在两种可能,①NO、②为O2,依据化学方程式分析.
解答 解:NO、O2和水反应生成硝酸,化学方程式为:4NO+3O2+2H2O=4HNO3,NO的量相对于氧气不足,剩余气体不可能为NO,剩余气体为O2,12mlNO完全反应,同时消耗的氧气的体积为12ml×$\frac{3}{4}$=9ml,剩余氧气3mol;
A、剩余气体不可能为NO,剩余气体为O2,故A错误;
B、剩余气体不可能为NO,剩余气体为O2,故B错误;
C、剩余的气体氧气,为无色的气体,故C错误;
D、试管内气体先是一氧化氮和氧气反应变为红棕色,后红棕色二氧化氮和水反应生成一氧化氮,反复几次,最后剩余无色气体氧气,故D正确.
故选D.
点评 本题考查NO、O2和水的反应,侧重于学生的分析能力和计算能力的考查,明确发生的化学反应,结合方程式计算是解答本题的关键,难度中等.

练习册系列答案
相关题目
13.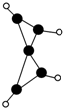 科学家最近在-100℃的低温下合成一种烃X,此分子的结构如图所示(图中的连线表示化学键).下列说法正确的是( )
科学家最近在-100℃的低温下合成一种烃X,此分子的结构如图所示(图中的连线表示化学键).下列说法正确的是( )
 科学家最近在-100℃的低温下合成一种烃X,此分子的结构如图所示(图中的连线表示化学键).下列说法正确的是( )
科学家最近在-100℃的低温下合成一种烃X,此分子的结构如图所示(图中的连线表示化学键).下列说法正确的是( )| A. | X既能使溴的四氯化碳溶液褪色又能使酸性KMnO4溶液褪色 | |
| B. | X是一种常温下能稳定存在的液态烃 | |
| C. | X和乙烷类似,都容易发生取代反应 | |
| D. | 充分燃烧等质量的X和甲烷,甲烷消耗氧气较多 |
14.类推的思维方式在化学学习与研究中经常采用,但类推出的结论是否正确最终要经过实践的验证.以下类推的结论正确的是( )
| A. | 氢气能还原氧化铜中的铜,铜能还原硝酸银溶液中的银,所以,氢气也能还原硝酸银溶液产生金属银 | |
| B. | CO2与SiO2化学式相似,故CO2与SiO2的结构、性质也相似 | |
| C. | 由“2Fe+3Cl2=2FeCl3”反应可推出“2Fe+3I2=2FeI3”反应也能发生 | |
| D. | K与Na同主族并位于Na的下方,Na常温下能与水剧烈反应,故K常温下也能与水剧烈反应 |
18.在一密闭容器中,反应aA(g)?bB(g)达到平衡后,保持温度不变,将容器体积缩小到原体积的一半,达到新的平衡后,B的浓度是原来的1.8倍,则( )
| A. | 平衡向正反应方向移动 | B. | 物质A的转化率减小 | ||
| C. | 物质B的质量分数增加 | D. | a>b |
8.以下表示正确的是( )
| A. | 明矾净水原理:Al3++3H2O═Al(OH)3↓+3H+ | |
| B. | 醋酸溶于水电离:CH3COOH?CH3COO-+H+ | |
| C. | 碳酸钠溶液水解:CO32-+H2O═HCO3-+OH- | |
| D. | 硫酸钡溶解于水中:BaSO4?Ba2++SO42- |
15.下列文字表述与反应方程式对应且正确的是( )
| A. | 溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+═AgBr | |
| B. | 乙醛溶液中加入足量的银氨溶液并加热CH3CHO+2$Ag(N{H}_{3}{)_{2}}^{+}$$\stackrel{水溶加热}{→}$$C{H}_{3}CO{O}^{-}$+$N{H}_{4}^{+}$+3NH3+2Ag↓+H2O | |
| C. | 向苯酚钠溶液中通入少量二氧化碳CO2+H2O+2C6H5O-→2C6H5OH+CO32- | |
| D. | 实验室用浓溴水检验苯酚: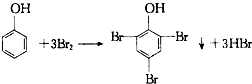 |
12.不慎接触到敌敌畏或甲胺磷时可以用碱性溶液处理因为它们是( )
| A. | 醛类 | B. | 有机物 | C. | 酯类 | D. | 盐类 |
13.下列说法正确的是( )
| A. | 药品柜的同一层不可存放浓硝酸和浓氨水 | |
| B. | 保存在无色玻璃试剂瓶中的浓硝酸要放在阴凉处 | |
| C. | 铵态氮肥可与草木灰混合雨天施用 | |
| D. | 固氮就是将氮元素转化成固体 |
