题目内容
下列溶液能用来区别SO2和CO2气体的是
| A.石灰水 | B.酚酞溶液 | C.BaCl2溶液 | D.品红溶液 |
D
解析试题分析:A、SO2和CO2为酸性氧化物,通入石灰水中均产生白色沉淀,过量白色沉淀消失,现象相同,无法鉴别,错误;B、SO2和CO2为酸性氧化物,通入酚酞溶液中均无明显现象,无法鉴别,错误;C、SO2和CO2通入BaCl2溶液均无明显现象,无法鉴别,错误;D、SO2具有漂白性,通入品红溶液中溶液褪色,CO2不能,可以鉴别,正确。
考点:考查SO2和CO2的鉴别。

练习册系列答案
相关题目
如图所示,A处通入氯气,关闭旋塞B时,C处红色布条无明显的变化,打开旋塞B时,C处红色布条逐渐褪色。由此作出的判断正确的是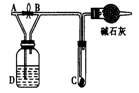
| A.D中不可能是浓硫酸 | B.D中可以是水 |
| C.通入的氯气中含有水蒸气 | D.D中可以是饱和食盐水 |
关于硅及其化合物的叙述中,不正确的是
| A.硅是良好的半导体材料 |
B.二氧化硅能与石灰石反应:SiO2+CaCO3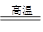 CaSiO3+CO2↑ CaSiO3+CO2↑ |
C.可以用焦炭还原二氧化硅生产硅:SiO2+2C 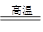 Si +2CO↑ Si +2CO↑ |
| D.水泥的主要成分是 Na2SiO3、CaSiO3和 SiO2 |
一种盐X与氢氧化钠溶液共热,可放出气体Y,Y经过一系列氧化后再溶于水可得Z溶液,Y和Z溶液反应又生成X,则X可能是
| A.NH4NO3 | B.NH4Cl | C.NH4HCO3 | D.(NH4)2CO3 |
NH4HCO3是一种离子化合物,下列关于该物质的叙述错误的是
| A.所含四种元素的原子半径由小到大的顺序为:H<O<N<C |
| B.同周期的三种元素的得电子能力由大到小的顺序为: O>N>C |
| C.除去NaCl固体中混有少量的NH4HCO3固体可以采用加热的方法 |
D.其与足量氢氧化钠溶液共热的离子方程式为:NH4++OHˉ NH3↑+H2O NH3↑+H2O |
向50 mL 18 mol·LH2SO4溶液中加入足量的铜片并加热。充分反应后,被还原的H2SO4的物质的量是
| A.小于0.45 mol | B.等于0.45 mol |
| C.在0.45 mol和0.9 mol之间 | D.大于0.9 mol |
下列气体有颜色和有刺激性气味的是
| A.CO2 | B.Cl2 | C.O2 | D.CO |
将SO2通入 BaCl2溶液至饱和,未见沉淀生成,继续通入另一种气体,仍无沉淀,则通入的气体可能是( )
| A.CO2 | B.NH3 | C.NO2 | D.Cl2 |
对于下列事实的解释错误的是( )。
| A.常温下,浓硫酸可以用铝罐贮存,说明铝与浓硫酸不反应 |
| B.浓硝酸在光照的条件下颜色变黄,说明浓硝酸不稳定 |
| C.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 |
| D.反应CuSO4+H2S=CuS↓+H2SO4能进行,说明硫化铜既不溶于水,也 |