题目内容
如图所示,A处通入氯气,关闭旋塞B时,C处红色布条无明显的变化,打开旋塞B时,C处红色布条逐渐褪色。由此作出的判断正确的是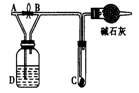
| A.D中不可能是浓硫酸 | B.D中可以是水 |
| C.通入的氯气中含有水蒸气 | D.D中可以是饱和食盐水 |
C
解析试题分析:潮湿的氯气具有漂白性,干燥的氯气不具备漂白性。根据题意知,A处通入氯气,关闭旋塞B时,C处红色布条无变化,打开旋塞B时,C处红色布条褪色,说明通入的氯气中含有水蒸气,氯气和水反应生成次氯酸起漂白作用,遇到有色布条使其褪色;A、D中可能是浓硫酸,吸收氯气中的水蒸气,干燥的氯气不能漂白有色布条,所以C处红色布条无变化,错误;B、D中为水时,氯气通过后会含有水蒸气,会使有色布条褪色,错误;C、A处通入氯气,关闭旋塞B时,C处红色布条无变化,打开旋塞B时,C处红色布条褪色,说明通入的氯气中含有水蒸气,正确;D、D中是饱和食盐水时,氯气通过后会含有水蒸气,会使有色布条褪色,错误。
考点:考查氯气的化学性质。

练习册系列答案
 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
硅及其化合物在材料领域中应用广泛。下列叙述中不正确的是( )
| A.硅单质可用来制造太阳能电池 |
| B.装碱性溶液的玻璃试剂瓶不能用玻璃塞 |
| C.二氧化硅是制造光导纤维的材料 |
| D.二氧化硅属于酸性氧化物,不能与任何酸反应 |
有关氨气的说法正确的是
| A.氨气与氯气相遇可能冒白烟 |
| B.氨气通入浓硫酸或浓硝酸中会被氧化 |
| C.氨气可以由所有铵盐受热分解得到 |
| D.氨气比PH3易液化是因为N?H键的键能比P?H键能大 |
硅及其化合物在材料领域中应用广泛,下列叙述正确的是
| A.硅单质是制造玻璃的主要原料 |
| B.CaSiO3可用来制造太阳能电池 |
| C.水泥的主要成分是Na2SiO3、CaSiO3和SiO2 |
| D.二氧化硅是制造光导纤维的材料 |
下列溶液能用来区别SO2和CO2气体的是
| A.石灰水 | B.酚酞溶液 | C.BaCl2溶液 | D.品红溶液 |
下列关于硅酸盐工业的叙述正确的是
| A.普通玻璃的主要成分可以表示为Na2O·CaO·6SiO2,说明玻璃为纯净物 |
| B.陶瓷、玻璃、水泥都属于硅酸盐产品 |
| C.制玻璃、水泥时都用到了石灰石和黏土 |
D.制玻璃的过程中发生了反应:Na2CO3+SiO2 Na2SiO3+CO2↑,说明酸性:H2SiO3>H2CO3 Na2SiO3+CO2↑,说明酸性:H2SiO3>H2CO3 |
如图是一种检验某气体化学性质的实验装置,图中B为开关,如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去。则D瓶中盛有的溶液是( )
| A.浓硫酸 | B.饱和NaCl溶液 |
| C.浓NaOH溶液 | D.浓NaBr溶液 |
下列说法不正确的是( )
| A.活性炭、SO2、Na2O2都能使品红溶液褪色,但原理不同 |
| B.同温同压下,两份相同质量的铁粉,分别与足量的稀硫酸和稀硝酸反应,产生气体的体积不相等 |
| C.将SO2气体通入BaCl2溶液中至饱和,未见沉淀生成,继续通入NO2则有沉淀生成 |
| D.将足量Cl2通入NaBr、NaI的混合溶液中,反应后将溶液蒸干并充分灼烧,剩余的固体物质成分为NaCl |