题目内容
美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金作载热介质,有关说法不正确的是( )
| A.合金的熔点一般比组分金属低 |
| B.铝钠合金若投入一定量的水中可完全溶解得无色溶液,则n(Al)≤n(Na) |
| C.铝钠合金投入到足量氯化铜溶液中,会有氢氧化铜沉淀也可能有铜析出 |
| D.若m g不同组成的铝钠合金投入足量盐酸中,放出的H2越多,则铝的质量分数越小 |
D
解析试题分析:A、根据合金的概念和性质知,合金的熔点一般比组分金属低,正确;B、铝钠合金若投入一定量的水中发生的反应为:2Na+2H2O====2NaOH+H2↑,2Al+2NaOH+2H2O====2NaAlO2+3H2↑,若完全溶解得无色溶液,则n(Al)≤n(Na),正确;C、铝钠合金投入到足量氯化铜溶液中,钠和水反应生成的氢氧化钠可以和氯化铜反应生成氢氧化铜沉淀,若n(Al)>n(Na),金属铝也可能会置换出金属铜,正确;D、根据金属钠和金属铝和酸反应生成氢气的定量关系:2Al——3H2,2Na——H2知,等质量的金属钠和金属铝,则金属铝产生的氢气量多,放出的H2越多,则铝的质量分数越大,错误。
考点:考查合金的概念和性质、钠和铝的性质。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
观察是研究物质性质的一种基本方法.一同学将一小块金属钠露置于空气中,观察到下列现象:银白色→①变灰暗→②变白色→③出现液滴→④白色固体,下列说法中正确的是 ( )
| A.①发生了氧化还原反应 | B.②变白色是因为生成了碳酸钠 |
| C.③是碳酸钠吸收空气中的水蒸气形成了溶液 | D.④只发生物理变化 |
下列物质中,不与盐酸反应,但可与氢氧化钠溶液反应的是
| A.Al(OH)3 | B.Al2O3 | C.SiO2 | D.Al |
下列有关物质用途的说法中,正确的是
| A.氨气是生产硝酸的重要原料 | B.甲烷与氯气反应可制得纯净的一氯甲烷 |
| C.铁制容器可用来盛放稀硝酸 | D.油脂经皂化反应可获得高级脂肪酸 |
有一镁、铝合金,用适量稀硫酸恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随氢氧化钠的体积关系如图所示,则原合金中镁、铝物质的量比为 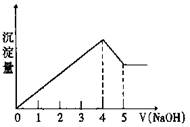
| A.2∶1 | B.4∶1 | C.1∶1 | D.1∶2 |
要使金属晶体熔化必须破坏其中的金属键。金属晶体熔、沸点高低和硬度大小一般取决于金属键的强弱。由此判断下列说法正确的是
| A.金属镁的熔点高于金属铝 |
| B.碱金属单质的熔、沸点从Li到Cs是逐渐升高的 |
| C.金属镁的硬度小于金属钙 |
| D.金属铝的硬度大于金属钠 |
将15.6gNa2O2和5.4gAl同时放入一定量的水中,充分反应后得到200mL澄清溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72L,若反应过程中溶液的体积保持不变,则
| A.反应过程中得到6.72L的气体(标准状况下) |
| B.最终得到的溶液中c(Na+)=c(Cl-)+c(OH-) |
| C.最终得到7.8g的沉淀 |
| D.最终得到的溶液中c(NaCl)=1.6 mol/L |