题目内容
15.在标准状况下,由CO和CO2组成的混合气体8.96L,质量是16g.此混合物中CO和CO2的物质的量比是1:3,C和O的原子个数比是2:9,CO的体积分数是0.25,CO的质量分数是17.5%,混合气体的平均摩尔质量是40g/mol.分析 根据n=$\frac{V}{{V}_{m}}$计算CO和CO2组成的混合气体的物质的量,列方程计算CO和CO2各自物质的量,可得二者物质的量之比,结合每个分子含有原子数目计算原子数目之比;体积分数等于物质的量分数;根据m=nM计算CO质量,再根据质量分数定义计算CO质量分数;根据$\overline{M}$=$\frac{{m}_{总}}{{n}_{总}}$计算平均摩尔质量.
解答 解:CO和CO2组成的混合气体的物质的量为$\frac{8.96L}{22.4L/mol}$=0.4mol,
设CO和CO2的物质的量分别为xmol、ymol,则:
$\left\{\begin{array}{l}{x+y=0.4}\\{28x+44y=16}\end{array}\right.$
解得x=0.1、y=0.3
故CO和CO2的物质的量之比为0.1mol:0.3mol=1:3,
含有原子数目之比为1×2:3×3=2:9,
CO的体积分数为$\frac{0.1mol}{0.1mol+0.3mol}$=0.25,
CO质量为0.1mol×28g/mol=2.8g,CO质量分数为$\frac{2.8g}{16g}$×100%=17.5%;
平均摩尔质量为$\frac{16g}{0.4mol}$=40g/mol,
故答案为:1:3;2:9;0.25;17.5%;40g/mol.
点评 本题考查物质的量有关计算,比较基础,注意对公式的理解与灵活应用.

练习册系列答案
相关题目
5.下列说法正确的是( )
| A. | CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2,故反应一定是吸热反应 | |
| B. | 在101 kPa时,1 mol碳燃烧所放出的热量为碳的燃烧热 | |
| C. | 物质燃烧都需要氧气 | |
| D. | 物质燃烧放出热最的多少与外界条件有关 |
6.已知柠檬醛的结构简式如图:根据你所学的知识,下列说法不正确的是( )


| A. | 它可以使酸性KMnO4溶液褪色 | |
| B. | 它可以与银氨溶液反应 | |
| C. | 它可以使溴水褪色 | |
| D. | 它可被催化加氢,最后产物是C10H20O |
3.从樟科植物枝叶提取的精油中含有如图1甲、乙和如表丙三种成分:

(1)甲和乙中含氧官能闭的纪称为羟基,醛基.1mol甲最多可以和4molH2发生加成反应.
(2)由甲可以制取高聚物K,请写出该反应的方程式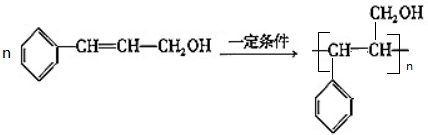
(3)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
甲$→_{Ⅰ}^{一定条件}$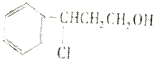 $→_{△}^{O_{2}/Cu}$Y$→_{Ⅱ}^{一定条件}$乙
$→_{△}^{O_{2}/Cu}$Y$→_{Ⅱ}^{一定条件}$乙
其中反应Ⅰ的反应类型为加成反应,反应Ⅱ的化学方程式为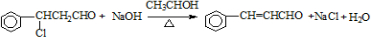 (注明反应条件).
(注明反应条件).
(4)已知:RCH=CHR′$→_{ii.Zn/H_{2}O}^{i.O_{3}}$RCHO+R′CHO;2HCHO$→_{ii.H+}^{i.浓NaOH}$HCOOH+CH3OH
由乙制丙的一种合成路线图如图2(A~F均为有机物,图中Mr表示相对分子质量):
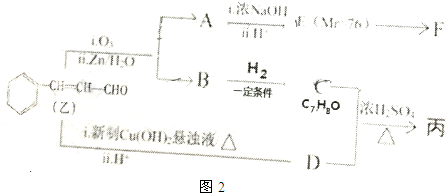
①C与D发生酯化反应生成丙,则丙的结构简式为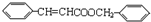 .
.
②下列物质不能与C反应的是bc(选填序号)
a.金属钠 b.氢氧化钠 c.Na2CO3溶液 d.乙酸
③F是由两分子E生成的六元环,写出F的结构简式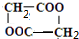 .
.
④同时符合以下条件的D的同分异构体有10种,
a.苯环上有三个取代基 b.能发生银镜反应 c.能与Br2的CCl4溶液发生加成反应 d.属于酚类
写出其中任意一种的结构简式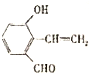 .
.

| 丙分子式 | C16H14O2 |
| 部分性质 | 能使Br2/CCl4褪色 |
| 能在稀H2SO4中水解 |
(2)由甲可以制取高聚物K,请写出该反应的方程式

(3)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
甲$→_{Ⅰ}^{一定条件}$
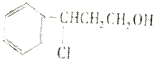 $→_{△}^{O_{2}/Cu}$Y$→_{Ⅱ}^{一定条件}$乙
$→_{△}^{O_{2}/Cu}$Y$→_{Ⅱ}^{一定条件}$乙其中反应Ⅰ的反应类型为加成反应,反应Ⅱ的化学方程式为
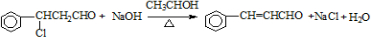 (注明反应条件).
(注明反应条件).(4)已知:RCH=CHR′$→_{ii.Zn/H_{2}O}^{i.O_{3}}$RCHO+R′CHO;2HCHO$→_{ii.H+}^{i.浓NaOH}$HCOOH+CH3OH
由乙制丙的一种合成路线图如图2(A~F均为有机物,图中Mr表示相对分子质量):

①C与D发生酯化反应生成丙,则丙的结构简式为
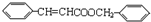 .
.②下列物质不能与C反应的是bc(选填序号)
a.金属钠 b.氢氧化钠 c.Na2CO3溶液 d.乙酸
③F是由两分子E生成的六元环,写出F的结构简式
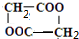 .
.④同时符合以下条件的D的同分异构体有10种,
a.苯环上有三个取代基 b.能发生银镜反应 c.能与Br2的CCl4溶液发生加成反应 d.属于酚类
写出其中任意一种的结构简式
 .
.
7. 25℃时,电离平衡常数:
25℃时,电离平衡常数:
回答下列问题:
(1)物质的量浓度为0.1mol.L-1的下列4种物质,pH由大到小的顺序是A>B>D>C.
A.Na2CO3
B.NaClO
C.CH3COONa
D.NaHCO3
(2)若增大氯水中次氯酸的浓度,可向氯水中加入的物质是BD.
A.Na2CO3
B.NaClO
C.CH3COONa
D.NaHCO3
(3)常温下0.1mol.L-1的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是A.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+).c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(4)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如下图所示,则HX的电离平衡常数大于(填“大于”“等于”或“小于”)醋酸的平衡常数;稀释后,HX溶液中水电离出来的c(H+)大于醋酸溶液水电离出来c(H+)(填“大于”“等于”或“小于”).
(5)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=9.9×10-7mol/L.(填准确数值)
 25℃时,电离平衡常数:
25℃时,电离平衡常数:| 弱酸化学式 | CH3COOH | HClO | H2CO3 |
| 电离平衡常数(25℃) | 1.75×10-5 | 3.0×10-8 | K1=4.4×10-7 K2=4.7×10-11 |
(1)物质的量浓度为0.1mol.L-1的下列4种物质,pH由大到小的顺序是A>B>D>C.
A.Na2CO3
B.NaClO
C.CH3COONa
D.NaHCO3
(2)若增大氯水中次氯酸的浓度,可向氯水中加入的物质是BD.
A.Na2CO3
B.NaClO
C.CH3COONa
D.NaHCO3
(3)常温下0.1mol.L-1的CH3COOH溶液加水稀释过程,下列表达式的数据一定变小的是A.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+).c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(4)体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如下图所示,则HX的电离平衡常数大于(填“大于”“等于”或“小于”)醋酸的平衡常数;稀释后,HX溶液中水电离出来的c(H+)大于醋酸溶液水电离出来c(H+)(填“大于”“等于”或“小于”).
(5)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=9.9×10-7mol/L.(填准确数值)
5.某有机物中碳、氢、氧质量比值为12:3:8,其质荷比图(图1)和核磁共振氢谱图(图2)分别如下,则该物质的结构简式为( )


| A. | CH3OCH3 | B. | CH3CH2OH | C. | CH3COOH | D. | CH3OH |
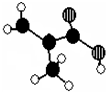
 ,W是否存在顺反异构?否 (填“是”或“否”).
,W是否存在顺反异构?否 (填“是”或“否”).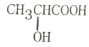 是W与水在一定条件下发生加成反应的产物的同系物.
是W与水在一定条件下发生加成反应的产物的同系物.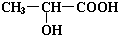 +2Na→
+2Na→ +H2↑.
+H2↑.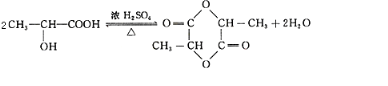 .
.