题目内容
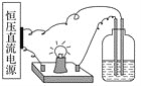
【题目】将以下4份溶液分别置于如图的装置中,其它条件相同时,灯泡最亮的是
A. 100 mL 1 mol·L-1的盐酸
B. 100 mL 2 mol·L-1的蔗糖溶液
C. 100 mL 1 mol·L-1的醋酸溶液
D. 30 mL 1 mol·L-1的氯化铝溶液
【答案】D
【解析】
溶液的导电性由离子浓度、离子电荷决定,其它条件相同时,溶液中的自由移动的离子的浓度越大、离子所带的电荷越多,则灯泡越亮。
结合上述分析知:A、氯化氢是强电解质,该溶液中的离子总浓度是2mol/L;B、蔗糖是非电解质,在溶液中以分子存在,不能导电;C、醋酸是弱电解质,该溶液中自由移动的离子浓度很小,故导电能力很弱;D、氯化铝是强电解质,在水溶液里完全电离,该反应中总的离子浓度是4mol/L,且铝离子带3个单位的正电荷;通过以上分析知,离子浓度最大的是氯化铝溶液,则氯化铝溶液中灯泡最亮。答案:D。

练习册系列答案
相关题目
【题目】700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+ H2O(g)![]() CO2 (g)+ H2(g)反应过程中测定的部分数据见下表(表中t2>t1):
CO2 (g)+ H2(g)反应过程中测定的部分数据见下表(表中t2>t1):
反应时间/min | n(CO)/mol | n(H2O)/mol |
0 | 1.20 | 0.60 |
t1 | 0.80 | |
t2 | 0.20 |
下列说法正确的是( )
A. 反应在t1min内的平均速率为![]()
B. 保持其他条件不变,起始时向容器中充入0.60molCO和1.20 molH2O,到达平衡时n(CO2)= 0.40mol
C. 保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时H2O转化率增大
D. 温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应



