题目内容
(13分)根据所学知识填空
(1)第二周期第VIA族的元素是第几号元素?
(2)核电荷数为13的元素在周期表中的位置第 周期第 族
(3)原子核内有10个质子的原子
(4)核外有10个电子的+2价阳离子
(5)核外有18个电子的一1价阴离子
(6)L层为最外层,L层的电子数是K层的3倍的原子 。
下面几题用“>”或“<”回答下列问题:
(7)酸性:H2CO3 H2SiO3 , H2SiO3 H3PO4
(8)碱性:Ca(OH)2 Mg(OH)2 ,Mg(OH)2 Al(OH)3.
(9)气态氢化物稳定性:H2O H2S , H2S HCl 。
(1)第二周期第VIA族的元素是第几号元素?
(2)核电荷数为13的元素在周期表中的位置第 周期第 族
(3)原子核内有10个质子的原子
(4)核外有10个电子的+2价阳离子
(5)核外有18个电子的一1价阴离子
(6)L层为最外层,L层的电子数是K层的3倍的原子 。
下面几题用“>”或“<”回答下列问题:
(7)酸性:H2CO3 H2SiO3 , H2SiO3 H3PO4
(8)碱性:Ca(OH)2 Mg(OH)2 ,Mg(OH)2 Al(OH)3.
(9)气态氢化物稳定性:H2O H2S , H2S HCl 。
(13分)(每空1分)
(1) 8 (2) 三 IIIA (3) Ne (4) Mg2+
(5)Cl- (6)O (7)> < (8)> > (9)> <
(1) 8 (2) 三 IIIA (3) Ne (4) Mg2+
(5)Cl- (6)O (7)> < (8)> > (9)> <
(1)(2)核电荷数为13的元素原子结构示意图: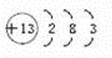 ,根据元素的核外电子层数=周期序数,最外层电子数=主族序数;
,根据元素的核外电子层数=周期序数,最外层电子数=主族序数;
(3)质子数=核电荷数=原子序数;
(4)对于阳离子:质子数=核外电子数+电子数,该元素为镁;
(5)对于阴离子:质子数=核外电子数-电子数,该元素为氯。
(7)酸性强弱比较:元素的非金属性越强,所对应的最高价氧化物的水化物酸性越强;元素的非金属性越强,所对应的气态氢化物越稳定;
(8)碱性强弱比较:元素的金属性越强,所对应的最高价氧化物的水化物碱性越强
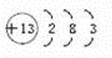 ,根据元素的核外电子层数=周期序数,最外层电子数=主族序数;
,根据元素的核外电子层数=周期序数,最外层电子数=主族序数;(3)质子数=核电荷数=原子序数;
(4)对于阳离子:质子数=核外电子数+电子数,该元素为镁;
(5)对于阴离子:质子数=核外电子数-电子数,该元素为氯。
(7)酸性强弱比较:元素的非金属性越强,所对应的最高价氧化物的水化物酸性越强;元素的非金属性越强,所对应的气态氢化物越稳定;
(8)碱性强弱比较:元素的金属性越强,所对应的最高价氧化物的水化物碱性越强

练习册系列答案
 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
 ,每百吨
,每百吨 的形式存在。下列说法正确的是( )。
的形式存在。下列说法正确的是( )。 原子核内含有4个质子
原子核内含有4个质子 和
和