题目内容
(12)某元素R原子的核外电子数等于核内中子数,该元素的单质2.8g与氧气充分反应,生成6.0g的化合物RO2。请回答:
(1)元素R的原子序数是 。
(2)元素R的原子共有 个电子层,能量最低的电子层中共有 个电子。
(3)写出元素R的最高价氧化物对应水化物的化学式 ,它的酸性比碳酸的酸性 。
(1)元素R的原子序数是 。
(2)元素R的原子共有 个电子层,能量最低的电子层中共有 个电子。
(3)写出元素R的最高价氧化物对应水化物的化学式 ,它的酸性比碳酸的酸性 。
(1) 14 (2)3 (3)2 (4)H2SiO3 (5)弱
有质量守恒定律得出参加反应的氧气质量为6 g—2.8 g="3.2" g,物质的量为3.2/32mol="0.1" mol,所以产物RO2物质的量也为0.1 mol,则其摩尔质量为60 g/ mol,因而R的相对原子质量为60—32=28,即其质子数为14,此元素为硅元素,原子序数是14。

练习册系列答案
相关题目
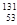 I),被人体超量吸入,可引发甲状腺疾病。下列说法正确的是( )
I),被人体超量吸入,可引发甲状腺疾病。下列说法正确的是( )