题目内容
【题目】下列有关氯元素及其化合物的表示正确的是( )
A.质子数为17、中子数为20的氯原子: ![]() Cl
Cl
B.氯离子(Cl﹣)的结构示意图: 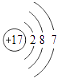
C.氯分子的电子式: ![]()
D.氯化氢的结构式:H﹣Cl
【答案】CD
【解析】解:A.质子数为17、中子数为20的氯原子质量数为37,该原子正确的表示方法为:1737Cl,故A错误;
B. 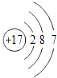 为氯原子结构示意图,氯离子的最外层达到8电子稳定结构,氯离子正确的离子结构示意图为:
为氯原子结构示意图,氯离子的最外层达到8电子稳定结构,氯离子正确的离子结构示意图为: 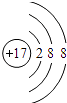 ,故B错误;
,故B错误;
C.氯分子中含有1个Cl﹣Cl键,其电子式为 ![]() ,故C正确;
,故C正确;
D.HCl为共价化合物,分子中含有H﹣Cl键,其结构式为:H﹣Cl,故D正确;
故选CD.
A.质量数=质子数+中子数,元素符号的左上角为质量数;
B.氯离子的核外电子总数为18,最外层满足8电子稳定结构;
C.氯气分子中含有1个Cl﹣Cl键,最外层满足8电子稳定结构;
D.用短线代替所有的共用电子对即为结构式,氯化氢分子中含有1个H﹣Cl键.

【题目】NaHSO3可被过量KIO3氧化,当NaHSO3完全消耗时才有I2析出。某课题组用0.02mol/LNaHSO3溶液和0.02mol/L KIO3溶液,以及淀粉作指示剂,通过测定溶液变蓝所用时间来探究影响化学反应速率的因素。
(1)写出NaHSO3溶液与过量KIO3溶液反应生成I2的离子方程式:__________________________。
(2)调节反应物浓度和温度进行对比实验,记录结果如下:
编号 | NaHSO3溶液(mL) | KIO3溶液(mL) | H2O(mL) | 反应温度(℃)/ | 变蓝时间(t/s) |
① | 10 | 15 | a | 10 | t1 |
② | 10 | 40 | 0 | 10 | t2 |
③ | 10 | b | 0 | 20 | t3 |
表中a=_________,b=_________。
(3)改变反应温度,重复实验③,得到温度(T)与溶液变蓝所需时间(t)的关系如下图所示(“×××”表示超过50℃后溶液不会再变蓝)。

①在30℃下,若溶液变蓝时,I2的物质的量为n mol,则从反应开始至溶液变蓝,IO3-的平均反应速率为_______mol·L-1·s-1(写出表达式即可,不要化简)。
②根据图像,请你描述低于50℃时,溶液变蓝所需时间与反应温度的关系:__________________。
(4)将NaHSO3溶液与KIO3溶液混合(预先加入可溶性淀粉为指示剂),用速率检测仪检测出起始阶段反应速率逐渐增大,一段时间后反应速率又逐渐减小。课题组在排除浓度、温度等影响因素后,对起始阶段反应速率逐渐增大的原因提出如下假设,请你完成假设二:
假设一:反应生成的I2对反应起催化作用;I2浓度越大反应速率越快;
假设二:________________________________________________________;
假设三:________________________________________________________;
(5)请你设计实验验证上述假设一,完成下表中内容(反应速率可用测速仪测定)。
实验方案 | 预期实验现象和结论 |
第一步:在烧杯甲中将NaHSO3溶液与过量KIO3 溶液混合, 用测速仪测定起始时的反应速率V(甲) 第二步:在烧杯乙中________________________,测定其起始阶段的相同时间内的反应速率V(乙) | 若__________,则假 设一成立 |