题目内容
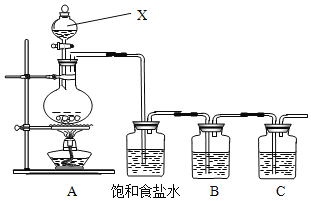
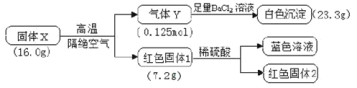
【题目】根据下图,回答问题。
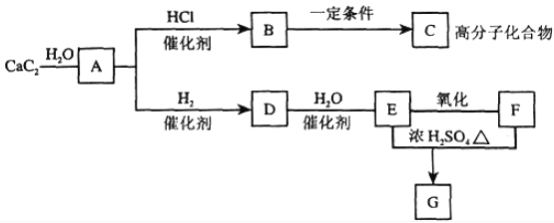
(1)有机物C的结构简式:________。
(2)①反应DE的化学方程式是_____________。
②E和F反应生成G的化学方程式是__________,反应类型为_________。
③实验室制取A的化学方程式__________。
【答案】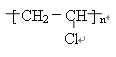 CH2=CH2+H2O
CH2=CH2+H2O![]() CH3CH2OH CH3COOH+CH3CH2OH
CH3CH2OH CH3COOH+CH3CH2OH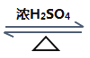 CH3COOCH2CH3+H2O 酯化反应(或取代反应) CaC2+2H2O→CH≡CH↑+Ca(OH)2
CH3COOCH2CH3+H2O 酯化反应(或取代反应) CaC2+2H2O→CH≡CH↑+Ca(OH)2
【解析】
由有机物的转化关系可知,CaC2与水反应生成氢氧化钙和乙炔,则A为乙炔;乙炔在催化剂作用下与HCl发生加成反应生成CH2=CHCl,则B为CH2=CHCl;CH2=CHCl一定条件下发生加聚反应生成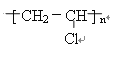 ,则C为
,则C为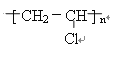 ;乙炔在催化剂作用下与H2发生加成反应生成CH2=CH2,则D为CH2=CH2;CH2=CH2在催化剂作用下与H2 O发生加成反应生成CH3CH2OH,则E为CH3CH2OH;CH3CH2OH催化氧化生成CH3COOH,则F为CH3COOH;在浓硫酸作用下,CH3CH2OH和CH3COOH发生酯化反应生成CH3COOCH2CH3,则G为CH3COOCH2CH3。
;乙炔在催化剂作用下与H2发生加成反应生成CH2=CH2,则D为CH2=CH2;CH2=CH2在催化剂作用下与H2 O发生加成反应生成CH3CH2OH,则E为CH3CH2OH;CH3CH2OH催化氧化生成CH3COOH,则F为CH3COOH;在浓硫酸作用下,CH3CH2OH和CH3COOH发生酯化反应生成CH3COOCH2CH3,则G为CH3COOCH2CH3。
(1)有机物C聚氯乙烯,结构简式为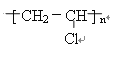 ,故答案为:
,故答案为: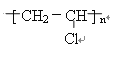 ;
;
(2)①反应DE为CH2=CH2在催化剂作用下与H2 O发生加成反应生成CH3CH2OH,反应的化学方程式为CH2=CH2+H2O![]() CH3CH2OH,故答案为:CH2=CH2+H2O
CH3CH2OH,故答案为:CH2=CH2+H2O![]() CH3CH2OH;
CH3CH2OH;
②E和F反应生成G的反应为在浓硫酸作用下,CH3CH2OH和CH3COOH发生酯化反应生成CH3COOCH2CH3,反应的化学方程式为CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O,故答案为:CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O,故答案为:CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O;酯化反应(或取代反应);
CH3COOCH2CH3+H2O;酯化反应(或取代反应);
③实验室用电石和乙炔反应制取乙炔,反应的化学方程式为CaC2+2H2O→CH≡CH↑+Ca(OH)2,故答案为:CaC2+2H2O→CH≡CH↑+Ca(OH)2。

【题目】位于前四周期的6种主族元素A、B、C、D、E、F原子序数依次增大,其中B、D同主族, D、E同周期。A、B、C在周期表中相邻,且三种元素的原子最外层电子数之和为18。F是其所在周期中最活泼的金属元素。根据推断回答下列问题:
(1)A在周期表中的位置_____;写出A单质的电子式________。
(2)用“>”或“<”填空:
离子半径 | 非金属性 | 酸性 | 氢化物的稳定性 |
F+_D2— | A_B | D的最高价氧化物的水化物___E的最高价氧化物的水化物 | C的氢化物__E的氢化物 |
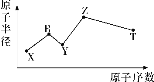
(3)—定条件,在水溶液中1molE-、![]() (x=1,2,3,4)的能量(KJ)相对大小如图所示。
(x=1,2,3,4)的能量(KJ)相对大小如图所示。
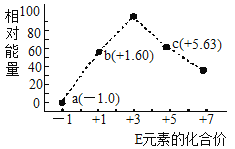
①c点对应的微粒是_______(填离子符号)。
②b→a+c反应的离子方程式为________,该反应是______反应(填“吸热”或“放热”)。