题目内容
11.质量相同的H2O和D2O所含质子数之比为10:9,中子数之比为8:9,分别与足量的金属钠反应生成气体在同温同压下体积之比为10:9.分析 根据n=$\frac{m}{M}$计算质量相同的H2O和D2O的物质的量之比,每个H2O含有10个质子、8个中子,每个D2O分子含有10个质子、10个质子,据此计算质子数、中子数之比;生成氢气的体积之比等于水的物质的量之比.
解答 解:根据n=$\frac{m}{M}$可知,质量相同的H2O和D2O的物质的量之比=20g/mol:18g/mol=10:9,每个H2O含有10个质子、8个中子,每个D2O分子含有10个质子、10个质子,故含有质子数之比为10×10:9×10=10:9,含有中子数之比10×8:9×10=8:9,生成氢气的体积之比等于水的物质的量之比,故二者分别与足量的金属钠反应生成气体在同温同压下体积之比为10:9,
故答案为:10:9;8:9;10:9.
点评 本题考查物质的量有关计算,注意对公式的理解与灵活应用,有利于基础知识的巩固.

练习册系列答案
相关题目
1.下列物质中,既能导电,又属于强电解质的一组是( )
| A. | 液态氯化钠、液态氯化氢 | B. | 熔融NaOH、熔融BaSO4 | ||
| C. | 石墨、分析纯盐酸 | D. | 冰醋酸、分析纯硫酸 |
2.将铁条插入下列溶液中,不会发生反应的是( )
| A. | 稀硫酸 | B. | 稀盐酸 | C. | 硝酸铜 | D. | 氢氧化钠 |
19.下列说法不正确的是( )
| A. | Al2O3用作耐火材料、Al(OH)3用作阻燃剂 | |
| B. | 碳素钢的主要成分是铁碳合金、司母戊鼎的主要成分是铜锡合金 | |
| C. | 自然界中不存在游离态的硅,硅主要以二氧化硅和硅酸盐的形式存在 | |
| D. | 通过化学变化可以实现12C与14C间的相互转化 |
16.下列电离方程式正确的是( )
| A. | BaSO4═Ba2++SO42- | |
| B. | Na2CO3═Na++CO32- | |
| C. | SO3溶于水溶液可以导电,故其属于电解质 | |
| D. | CaCO3投入水中,溶液不导电,说明CaCO3是非电解质 |
3.图装置,电流计指针会偏转,正极变粗,负极变细,符合这种情况的是( )
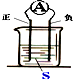

| A. | 正极:Cu 负极:Zn S:稀H2SO4 | |
| B. | 正极:Zn 负极:Cu S:CuSO4溶液 | |
| C. | 正极:Ag 负极:Zn S:AgNO3溶液 | |
| D. | 正极:Fe 负极:Cu S:AgNO3溶液 |
18.卤块的主要成分是MgCl2,此外还含有少量的Fe3+、Fe2+和Mn2+等离子,以卤块为原料制取轻质氧化镁工艺以及相关数据如图:
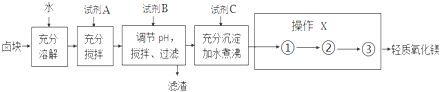
若要求产品尽量不含杂质,而且生产成本较低,请根据如表提供的资料,回答下列问题:
表1 生成氢氧化沉淀的pH
Fe2+氢氧化物呈絮状,不易从溶液中除去,所以,常将它氧化为 Fe3+,生成 Fe(OH)3沉淀除去
表2 原料价格表
(1)要使卤块充分溶解,可采取的措施有适当加热、搅拌、将卤块粉碎等(至少答2点)
(2)加入的试剂A,最佳的选择是漂液.
(3)为尽量除去杂质,试剂B为NaOH,当溶液的pH为9.8时,停止加入B.
(4)操作X中①②③步的操作分别是过滤、洗涤、灼烧、检验步骤②是否进行完全的操作是:取最后一次洗涤液少许做焰色反应.
(5)加入的试剂C是 Na2CO3,煮沸发生的反应方程式为MgCO3+H2O$\frac{\underline{\;加热煮沸\;}}{\;}$Mg(OH)2+CO2↑.

若要求产品尽量不含杂质,而且生产成本较低,请根据如表提供的资料,回答下列问题:
表1 生成氢氧化沉淀的pH
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
表2 原料价格表
| 物质 | 价格/(元•吨-1) |
| 漂液(含 25.2% NaClO) | 450 |
| 双氧水(含 30% H2O2) | 2400 |
| 烧碱(含 98% NaOH) | 2100 |
| 纯碱(含 99.5% Na2CO3) | 600 |
(2)加入的试剂A,最佳的选择是漂液.
(3)为尽量除去杂质,试剂B为NaOH,当溶液的pH为9.8时,停止加入B.
(4)操作X中①②③步的操作分别是过滤、洗涤、灼烧、检验步骤②是否进行完全的操作是:取最后一次洗涤液少许做焰色反应.
(5)加入的试剂C是 Na2CO3,煮沸发生的反应方程式为MgCO3+H2O$\frac{\underline{\;加热煮沸\;}}{\;}$Mg(OH)2+CO2↑.
 将5.3g某碱式碳酸盐固体(不含结晶水)M溶解于100g 9.8%的稀硫酸中,充分反应后得到224mL CO2(标准状况)和含有MgSO4、Al2(SO4)3的溶液.向所得溶液中逐滴加入NaOH溶液,产生沉淀的质量与加入的溶质NaOH的质量关系如图所示.
将5.3g某碱式碳酸盐固体(不含结晶水)M溶解于100g 9.8%的稀硫酸中,充分反应后得到224mL CO2(标准状况)和含有MgSO4、Al2(SO4)3的溶液.向所得溶液中逐滴加入NaOH溶液,产生沉淀的质量与加入的溶质NaOH的质量关系如图所示.