题目内容
(10分)利用天然气合成氨的工艺流程示意如下:
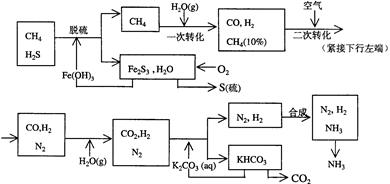
依据上述流程,完成下列填空:
(1)天然气脱硫时的化学方程式是
(2)n mol CH4经一次转化后产生CO 0.9n mol、产生H2 mol(用含n的代数式表示)
(3)K2CO3(aq)和 CO2反应在加压下进行,加压的理论依据是 (多选扣分)
(a)相似相溶原理 (b)勒沙特列原理 (c)酸碱中和原理
(4)由KHCO3分解得到的CO2可以用于 (写出CO2的一种重要用途)。

依据上述流程,完成下列填空:
(1)天然气脱硫时的化学方程式是
(2)n mol CH4经一次转化后产生CO 0.9n mol、产生H2 mol(用含n的代数式表示)
(3)K2CO3(aq)和 CO2反应在加压下进行,加压的理论依据是 (多选扣分)
(a)相似相溶原理 (b)勒沙特列原理 (c)酸碱中和原理
(4)由KHCO3分解得到的CO2可以用于 (写出CO2的一种重要用途)。
(1)3H2S+2Fe(OH)3=Fe2S3+6H2O (2)2.7n (3)b
(4)生产纯碱(或作制冷剂等,其它合理答案也给分)
(4)生产纯碱(或作制冷剂等,其它合理答案也给分)
试题分析:(1)根据图示可知,用Fe(OH)3脱去天然气中的H2S,所以反应的化学方程式为3H2S+2Fe(OH)3=Fe2S3+6H2O。
(2)CH4+H2O=CO+3H2,所以生成0.9n molCO时,生成H22.7nmol。
(3)K2CO3+H2O+CO2=2KHCO3,加压平衡正向移动,依据的原理是勒沙特列原理。
(4)CO2可以用来做制纯碱的原料。
点评:本题主要考查学生分析问题的能力,难度较小,综合性强。

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
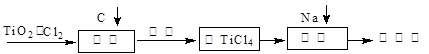
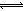 TiCl4(g)+2CO (g) 。试计算其反应的△H= kJ?mol-1;反应的平衡常数表达式K= ,在下图中作出TiCl4达到平衡后百分含量随温度的变化趋势图。
TiCl4(g)+2CO (g) 。试计算其反应的△H= kJ?mol-1;反应的平衡常数表达式K= ,在下图中作出TiCl4达到平衡后百分含量随温度的变化趋势图。
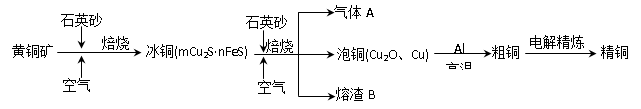
 2SO3(g),该反应的平衡常数表达式为K= ;过量的SO2与NaOH溶液反应的化学方程式为
2SO3(g),该反应的平衡常数表达式为K= ;过量的SO2与NaOH溶液反应的化学方程式为 