题目内容
(4分)有机物A由碳、氢、氧三种元素组成。现取2.3 g A与2.8 L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重2.7 g,碱石灰增重2.2 g。回答下列问题:
(1)2.3 g A中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式。
⑴2.3 g A中所含氢原子、碳原子的物质的量各是0.3mol、0.1mol ;
⑵该有机物的分子式为C2H6O。
解析试题分析:⑴解:n(O2)=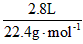 =0.125mol m(O2)=0.125 mol×32g·mol-1=4g
=0.125mol m(O2)=0.125 mol×32g·mol-1=4g
n(H2O)=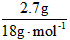 = 0.15mol n(CO2) =
= 0.15mol n(CO2) =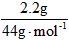 =0.05mol
=0.05mol
m(CO)=4g+2.3g-2.7g-2.2g=1.4g n(CO)=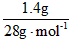 =0.05mol
=0.05mol
n(H)=2n(H2O)=0.15molx2=0.3mol;
n(C)=n(CO2)+n(CO)=0.05mol+0.05mol=0.1mol
⑵解:2.3g A中所含氧原子:
n(O)=(0.05mol×2+0.05mol+0.15mol)-0.125mol×2=0.05mol
n(C)∶n(H)∶n(O) =0.1mol∶0.3mol∶0.05mol=2∶6∶1
则A 的最简式为 C2H6O ,根据价键规则得 A的分子式为:C2H6O
考点:考查有机化学的计算。

10ml由两种有机物按等物质的量组成的混合气体,该混合气体完全燃烧需17.5ml的O2,并生成15ml的CO2和15ml的水蒸气(所有气体体积均在相同状况下测定)。
试在下表中填出所有可能组合(有多少填多少,不一定填满)。
| 第1组(两种有机物结构简式) | 第2组(两种有机物结构简式) | 第3组(两种有机物结构简式) | 第4组(两种有机物结构简式) |
| | | | |
某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯。
已知: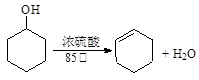 ;
;
反应物和生成物的物理性质如下表:
| | 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 |
| 环已醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环已烯 | 0.81 | -103 | 83 | 难溶于水 |
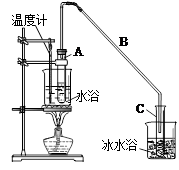
①A中碎瓷片的作用是 ,导管B除了导气外还具有的作用是 。
②试管C置于冰水浴中的目的是 。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入
饱和食盐水,振荡、静置、分层,环己烯在 层(填上
或下),分液后用 (填序号)洗涤:
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按下图装置蒸馏,冷却水从 (填字母)口进入;蒸馏时要加入生石灰的目的 。
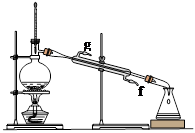
③上图蒸馏装置收集产品时,控制的温度应在 左右,实验制得的环己烯精品质量低于理论产量,可能的原因是 :a.蒸馏时从70℃开始收集产品;b.环己醇实际用量多了;c.制备粗品时环己醇随产品一起蒸出;d.是可逆反应,反应物不能全部转化
(3)区分环己烯精品和粗品(是否含有反应物)的方法是 。
乙酸正丁酯是一种重要化工原料,某实验小组利用图1、图2装置合成乙酸正丁酯(夹持装置已略去),发生的化学反应为: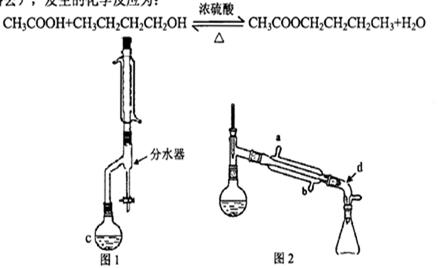
可能用到的有关数据见下表: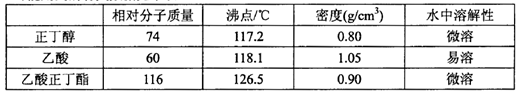
实验步骤如下:
①在图1的圆底烧瓶中,装入7.Og正丁醇和7.Og冰醋酸,再加入3-4滴浓硫酸。
②如图1所示,安装分水器和回流冷凝管。加热圆底烧瓶,待反应基本完成后,停止加誊
③冷却后将分水器中分出的酯层和圆底烧瓶中的反应液一起倒入分液漏斗中。先后用水、10%碳酸钠溶液洗涤。分离得到的酯层再用水洗涤后倒入锥形瓶中,加无水硫酸镁干燥。
④将干燥后的酯层倒入图2的蒸馏烧瓶中,加热蒸馏。收集124℃-126℃的馏分,称得质量为7.0g。
回答下列问题:
(1)图2冷凝管中冷水从____口流入(用字母表示);仪器d的名称是____。
(2)分液漏斗使用前须____并洗净备用。分离上下层液体时,应先____,然后打开活塞放出下层液体,上层液体从上口倒出。
(3)实验中产生的副产物的结构简式为____(任写一种)。用10%碳酸钠溶液洗涤的主要目的是____。
(4)实验中图1圆底烧瓶c的容积最适合的是____(选填字母)。
| A.25mL | B.50mL | C.250mL | D.500mL |
(6)实验中,乙酸正丁酯的产率为____%。
下列物质中,能使酸性高锰酸钾溶液褪色的是
| A.苯 | B.乙烷 | C.乙烯 | D.乙酸 |
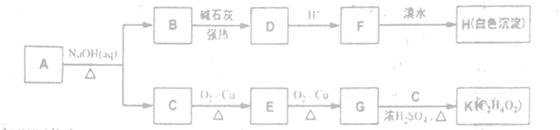
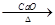 CH4↑+Na2CO3
CH4↑+Na2CO3