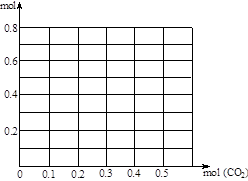题目内容
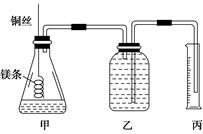
过碳酸钠俗称固体双氧水,是一种很好的消毒剂和供氧剂,化学式可表示为aNa2CO3·bH2O2,它具有Na2CO3和H2O2的双重性质。现将一定质量的过碳酸钠粉末溶于水配成稀溶液,再向其中加入适量的MnO2粉末,充分反应后生成672 mL气体(标准状况)。反应后的混合物经过滤、洗涤后,将滤液和洗涤液混合并加水配成100 mL溶液A。现向三份体积为10 mL、浓度为c的稀硫酸中分别逐滴滴入溶液A,边滴边振荡,充分反应后,测得实验数据如下表所示:
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 滴加溶液A的体积/mL | 5.0 | 10.0 | 15.0 |
| 生成气体的体积/mL(标准状况) | 44.8 | 89.6 | 112 |
请回答下列问题:
(1)用化学方程式表示向过碳酸钠溶液中加入MnO2粉末时放出气体的原因:_______________________________________________________________。
(2)稀硫酸的物质的量浓度c=________ mol·L-1。
(3)通过计算可确定过碳酸钠的化学式为________。
(4)工业上常以所含活性氧的质量分数
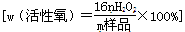 来衡量过碳酸钠产品的优劣,13%以上者为优等品。
来衡量过碳酸钠产品的优劣,13%以上者为优等品。现将0.2 g某厂家生产的过碳酸钠样品(所含杂质不参与后面的氧化还原反应)溶于水配成溶液,加入15.0 mL 1 mol·L-1硫酸,再加入足量KI,摇匀后置于暗处,充分反应后,加入少量淀粉试液,用0.1 mol·L-1 Na2S2O3溶液滴定到蓝色恰好消失时,共消耗33.00 mL,请通过计算判断该样品是否为优等品(要求写出计算过程)。(已知:2Na2S2O3+I2=Na2S4O6+2NaI)
(1)2H2O2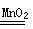 2H2O+O2↑
2H2O+O2↑
(2)0.5
(3)2Na2CO3·3H2O2
(4)据题意可得:H2O2+2I-+2H+=2H2O+I2,2Na2S2O3+I2=Na2S4O6+2NaI。根据关系式H2O2~2Na2S2O3可知,n(H2O2)=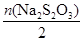 =
=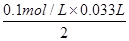 =1.65×10-3 mol
=1.65×10-3 mol
该过碳酸钠中活性氧的质量分数为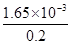 ×16×100%=13.2%>13%
×16×100%=13.2%>13%
所以该过碳酸钠样品为优等品。
解析

(1)900 K时,用足量的H2与钠钾合金10.10 g充分反应,得到10.40g白色的氢化物混合物,则该钠钾合金的化学式为____________。
(2)将l.56 g Na2O2加入20.00g水中,充分反应后,所得溶液的质量分数为________(保留3位小数,用百分数表示保留l位小数);25℃时NaOH的溶解度为53.00 g/100g水,则将该溶液蒸发_______g水后恢复至25℃可得饱和溶液(保留2位小数)。
(3)取10.00 gNaNO3加热,得到的固体中Na的质量分数为31.51%,则氧的质量分数为_________(保留2位小数)。
(4)某碱金属R与汞的合金2.4g加入足量水中,充分反应后,收集到气体l.12 L(标准状况),则可推导出R元素是________(写元素符号)。
(5)在l.12 L密闭容器中,将KOH与O3在一定条件下反应,得到气体(只含一种元素)、固体物质A和KOH·H2O。有关实验数据如下:
| KOH | O3 | A | KOH·H2O | 气体密度 |
| 16.8 g | 0.3 mol | a g | b g | >1.429 g/L |
| 16.8 g | 0.2 mol | a g | b g | 1.429 g/L |
A会缓慢分解产生一种钾的氧化物和O2。试确定A的化学式: 。
铁铝合金是一种新型高温结构材料。
(1)图9表示室温时不同组份的Fe3Al在65%浓HNO3 中的腐蚀情况。由图9可看出添加了 (填符号)元素的合金耐蚀性最差。
(2)高温条件下,Al和Fe2O3按一定比例混合反应可制
|
①小明同学提出如下方案:准确称取1.46g该合金粉末,再加入足量NaOH溶液(Si+2NaOH+H2O=Na2SiO3+2H2↑),充分反应后过滤,通过测定剩余固体质量及收集到气体的体积,可计算出此合金的组成。写出Al与NaOH溶液反应的离子方程式 。
②小军同学认为该方案难以测定标准状况下气体的体积,操作不简便。于是他设计了第二种方案:准确称取1.46g该合金粉末,加入过量盐酸溶液充分反应后过滤,测定剩余固体质量0.07g。向滤液中滴加足量浓NaOH溶液,充分搅拌、过滤、洗涤得固体。再将所得固体充分加热、灼烧得红棕色粉末1.60g。试通过计算确定此合金的组成。
氯化钠溶液在生产、生活中都有广泛的用途。现配置1 L 0.2 mol·L-1 NaCl溶液,请回答问题。
| 实验步骤 | 有关问题 |
| (1)计算并称量 | 用托盘天平称量NaCl固体的质量为 g |
| (2)溶解 | 为加速溶解,可进行的操作是 |
(3)转移 | 指出示意图中的两处错误: 错误1: 错误2: |
| (4)洗涤 | 用少量蒸馏水洗涤 2~3次,并将洗涤液转移到容量瓶中 |
| (5)定容 | 若俯视容量瓶刻度线,定容后会造成所配溶液的物质的量浓度 (填“偏高”“偏低”或“无影响”) |
用18.4mol·L-1的浓H2SO4配制100mL浓度为1mol·L-1的H2SO4溶液,其操作可分为以下各步:
| A.用量筒取 mL浓H2SO4缓缓注入装有约50mL蒸馏水的烧杯中,并用玻璃棒不断搅拌 |
| B.用约30mL蒸馏水,分成三次洗涤烧杯和玻璃棒,将每次洗液都倒入100mL容量瓶里 |
| C.将稀释后H2SO4溶液小心倒入100mL容量瓶里 |
| D.检查100mL容量瓶口部是否会发生滴漏 |
(F)盖紧瓶塞,反复颠倒振荡,摇匀溶液
(G)用 向容量瓶里逐滴滴入蒸馏水,至液面最低点恰好和环形刻度线相切
据此填写:(1)上述各步的空白处。
(2)正确的操作顺序是(字母填写) 。
(3)进行A步操作应选择下列量器:①10mL量筒;②50mL量筒;500mL量筒;④1000mL量筒中的(填序号) 。
分类是化学学习和研究的常用手段。下列分类依据和结论都正确的是
| A.HNO3、浓硫酸都具有强氧化性,都是氧化性酸 |
| B.H2O、CH3COOH、CaCO3均含有氧元素,都是氧化物 |
| C.HCl、CH3COOH、CH3CH2OH都易溶于水,都是电解质 |
| D.HCOOH、H2CO3、H2SO4分子中均含有两个氢原子,都是二元酸 |